1.埃博拉病毒(Orthoebolavirus zairense)
拉丁学名:Orthoebolavirus zairense
分类学地位:病毒域Riboviria;负链RNA病毒门Negarnaviricota;
单链负链病毒Monjiviricetes;单链负链病毒目Mononegavirales;
丝状病毒科Filoviridae;正埃博拉病毒属Orthoebolavirus
埃博拉病毒(Orthoebolavirus zairense)是正埃博拉病毒属中的代表性病毒株,也是引起埃博拉病毒病(Ebola virus disease, EVD)的主要病原体之一。该病毒具有典型的丝状体形态,基因组为单股负链RNA,能够感染人类及灵长类动物。EVD的传播方式主要通过直接接触患者的血液、体液或被污染的物品,亦可通过在医疗护理过程中缺乏防护措施而扩散。临床表现通常为急性起病,早期症状包括发热、头痛、肌肉痛、乏力等,随后可出现呕吐、腹泻和多器官功能损害,严重者可发展为出血性症状和休克。
1.1生物学特性
1.1.1培养特征
埃博拉病毒的体外生活史呈“细胞入侵-胞质复制-子代出芽”三阶段循环,全程在37°C、5% CO₂、2 % FBS-DMEM条件下即可在Vero E6、Huh7等灵长类细胞中完成,无需中间宿主或媒介[1]。
入侵:病毒以丝状颗粒水平或垂直接触细胞表面,通过GP与NPC1、整合素等受体结合,触发大胞饮途径进入胞质,该过程可被巨胞饮抑制剂显著阻断。
复制:核衣壳释放负链RNA,利用病毒自身L聚合酶在胞质内完成转录与基因组复制,NP、VP35、VP30等蛋白组装成新核衣壳,感染后24 h即可在上清中检出子代RNA。
出芽:GP经高尔基体修饰后转运至质膜,VP40介导核衣壳在膜上出芽并获得包膜,48–72 h形成典型CPE(细胞圆缩、合胞体、脱落),上清滴度可达10⁶–10⁷ TCID₅₀ mL⁻¹;整个周期3–4 d内完成,且对60°C 1 h、脂溶剂及含氯消毒剂敏感,故全部操作必须在BSL-4实验室进行。
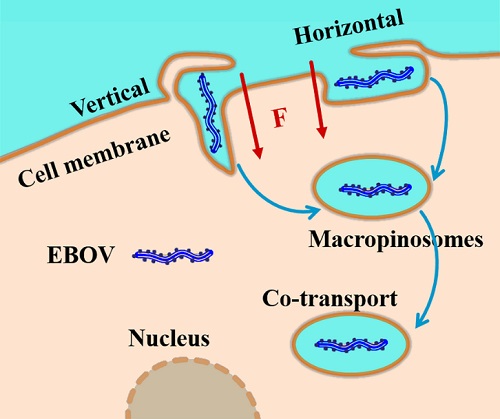
图1 单个埃博拉病毒入侵细胞动态示踪
1.1.2形态学特征
整体形态:病毒呈柔韧长丝状,体长800-1400 nm,最长可达14 µm,直径恒定80 nm;负染电镜下常弯曲成“U”“6”或闭合环状,两端钝圆或呈“鱼钩”样回折,表面糖蛋白突起密集排列,赋予刷状轮廓,这种波浪形态使其在黏滞的细胞外液中保持扩散能力并增加与靶膜的接触面积[2]。
内部结构:核衣壳位于病毒中心,呈螺旋对称,直径约50 nm,由负链RNA与NP、VP35、VP30、L蛋白共同缠绕成直径10-12 nm的致密轴心,外15 nm 厚的VP40基质层,形成“内管-外鞘”构造,为基因组提供机械支撑并充当膜出芽的适配平台[3]。
表面突起:包膜上镶嵌三聚体GP1/GP2刺突,长约7-10 nm,顶端球状头部直径4 nm,通过柔性铰链与茎部相连,电镜下呈“蘑菇”状,密度约每100 nm² 1–2个,整体覆盖病毒表面积20-30%;GP1负责受体结合,GP2介导低pH触发的膜融合,其高度糖基化的黏蛋白样区可遮蔽关键表位,使病毒在宿主免疫环境中实现隐身与高效侵袭[2]。
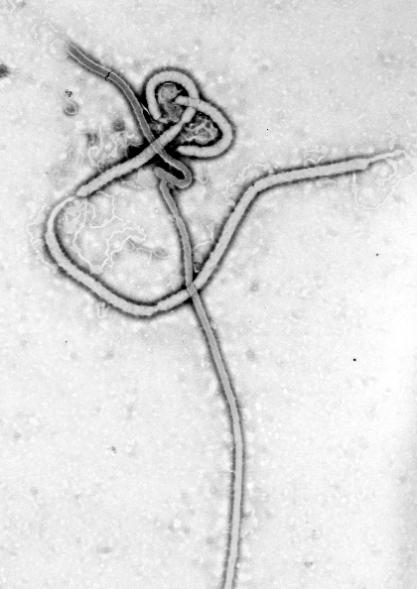
图2 电子显微镜下的埃博拉病毒颗粒
1.1.3生化特征
埃博拉病毒是一种丝状、包膜的非分节负链单股RNA病毒,基因组约19 kb,编码七个主要基因并表达出多种功能性蛋白:核蛋白(NP)与VP35/VP24共同组装成螺旋状核衣壳以包裹基因组并在胞质中形成复制/转录的包涵体;大蛋白L为依赖RNA的RNA聚合酶负责转录与复制,VP30为转录激活因子,VP35既是聚合酶辅因子又具有拮抗宿主干扰素反应的功能;基质蛋白VP40驱动病毒的膜关联聚合与出芽并决定丝状粒子的形态;外膜糖蛋白GP在内质网/高尔基被翻译并经裂解成熟为功能性亚基(GP1/GP2),其高度糖基化的粘蛋白样区域和可分泌的sGP既影响细胞受体结合与内吞/裂解后的NPC1受体识别,又参与免疫调节与病理学表现;总体上该病毒利用宏吞作用介导进入、经内体/溶酶体内的蛋白酶剪切曝光与NPC1结合引发膜融合释放核衣壳,完成胞质内复制与病毒装配出芽[4]。
1.1.4分子生物学特征
基因组与结构蛋白:埃博拉病毒属于单股负链非分节RNA病毒(non-segmented negative-sense, NNS RNA virus),基因组长度约19000核苷酸(约18.9-19.1 kb),不带5’端帽子(cap)和不带3’端poly-A尾;基因组中从3’到5’的主要编码顺序为:leader区→NP→VP35→VP40→GP/sGP→VP30→VP24→L→trailer区。leader和trailer是非翻译区,也包含调控复制/转录/基因包装的信号序列[5, 6]。
转录与复制机制:病毒进入宿主细胞后,其核衣壳(包含NP+RNA+VP35+VP30+L)释放RNA基本框架,L蛋白(RNA依赖RNA聚合酶)在VP35辅助下进行两种活动:一种是转录生成mRNAs(带5’cap和polyadenylated的形式,以便翻译成蛋白);另一种是复制生成反义模板,然后用它再合成新一代基因组RNA[6]。转录起始需要VP30作辅因子,其磷酸化状态对能否重新启动转录非常关键。VP30作用类似于“开关”从转录状态向复制状态的转变[7]。L-VP35复合物与基因组3’末端的leader序列结合时,leader RNA在进入模板通道时会形成一个稳定的弯折构象,这个构象对于de novo的复制起始至关重要[8]。
1.2分布、传播与致病性
1.2.1分布与传播
地理分布:埃博拉病毒主要分布于非洲撒哈拉以南地区,特别是中非和西非。自1976年首次在苏丹和刚果(金)被发现以来,历次大规模暴发多见于刚果(金)、乌干达、几内亚、塞拉利昂和利比里亚等国。Zaire ebolavirus(EBOV)是主要致病种类,也是致死率最高的株型;Sudan ebolavirus(SUDV)在苏丹、乌干达等地流行;Bundibugyo ebolavirus(BDBV)主要在乌干达和刚果(金)暴发;Reston ebolavirus(RESTV)多见于菲律宾和中国,主要感染非人灵长类和猪,目前尚无证据表明对人类致病。
传播途径:埃博拉病毒的自然宿主被认为是果蝠(尤其是Rousettus属与Hypsignathus monstrosus等),人类常因接触感染蝙蝠或受感染的非人灵长类、猪等中间宿主而获得初次感染。病毒主要通过以下途径在人群中传播:
直接接触传播:与患者的血液、体液(呕吐物、粪便、精液、母乳、唾液、泪液)接触;间接接触传播:接触被污染的环境或物品(如针具、床单);
院内传播:缺乏有效防护的医护操作;
性传播:病毒可在幸存男性精液中长期存在(>1个月),构成潜在传播风险。
共感染现象:
在非洲流行地区,埃博拉病毒感染可与其他病原体(如疟原虫、HIV、肠道细菌等)共存,这会加重临床表现并增加诊断难度。
1.2.2致病性
埃博拉病毒通过多种分子机制破坏宿主免疫防御并引发多系统损伤,临床表现通常分为急性进展过程:
早期阶段(1–3天):表现为发热、头痛、肌痛、乏力等非特异性症状,类似流感。
进展期(4–10天):出现呕吐、腹泻、胸痛、皮疹,伴随肝肾功能异常,部分患者可发生出血表现(牙龈出血、呕血、黑便、皮下瘀斑)。
重症期(7–14天):高致死性与“细胞因子风暴”相关,机理包括:
免疫逃逸:VP35抑制干扰素产生,VP24阻断STAT1入核,削弱抗病毒反应;
血管损伤:GP在内皮细胞表达导致通透性升高;
系统性炎症反应:TNF-α、IL-6等过度释放引起多器官功能衰竭;
凝血异常:激活组织因子途径,引起播散性血管内凝血(DIC)。
不同种类的致病性存在差异:EBOV致死率可达50–90%;SUDV、BDBV致死率25–60%;RESTV在人类无明确致病性。
1.3检测方法
分子检测(RT-PCR):反转录聚合酶链反应(RT-PCR)是埃博拉病毒诊断的“金标准”。该方法通过逆转录病毒RNA并扩增特异性基因片段(如NP、VP40、L基因),能在症状出现早期(通常发病后1–3天)检测到病毒RNA。实时荧光定量RT-qPCR可进一步实现病毒载量定量分析,Ct值与病情严重程度相关(高病毒载量往往预示较差预后)。该方法灵敏度和特异性均在95%以上,适合疫情暴发时快速确诊和监测。但其局限性是需要专业实验室和冷链运输,不适合基层医疗机构独立开展。
抗原检测(ELISA快速检测):酶联免疫吸附试验(ELISA)可检测病毒结构蛋白(如VP40、GP)或其衍生抗原,常用于急性期样本(血液、血清、尿液)。该方法操作相对简便,数小时内即可得到结果,适合资源有限地区。近年来发展出的免疫层析快速诊断试剂(RDTs)可在15–30分钟内检测VP40抗原,但敏感性较RT-PCR低(尤其在病毒载量较低的早期病例中易出现假阴性)。因此,抗原检测常作为初筛手段,与RT-PCR联合使用可提高整体诊断效率。
1.4典型案例
2014–2016年的西非埃博拉疫情是人类历史上最严重的一次埃博拉病毒暴发,起源于几内亚东南部,并迅速扩散至利比里亚、塞拉利昂等国,甚至传播到欧洲和美国,最终报告约28600例病例和11325例死亡,平均病死率约40%,在利比里亚部分地区一度超过70%。分子流行病学分析表明,本次疫情由扎伊尔型埃博拉病毒Makona毒株引发,与此前毒株基因组同源性约97%,但在GP、VP35和L蛋白等关键区域出现了多处变异,其中GP蛋白的A82V变异被认为增强了病毒在人体细胞中的感染能力。临床表现方面,患者通常先出现发热、乏力、头痛和肌肉痛等非特异性症状,随后可发展为腹泻、呕吐和皮疹,部分病例进入出血和多器官衰竭阶段,确诊主要依赖实时荧光定量RT-PCR检测病毒RNA以及ELISA检测病毒抗原或宿主抗体。
在疫情防控上,由于西非国家公共卫生体系薄弱,早期病例识别和隔离延误导致疫情迅速失控,迫使国际社会采取紧急应对措施,包括建立埃博拉治疗中心(ETCs)、加强接触者追踪和安全埋葬规范。同时,该疫情也是新型干预手段的重要试验场,首次在临床应用了单克隆抗体组合疗法ZMapp,尽管样本有限但显示出一定疗效;更为关键的是,加速推动了rVSV-ZEBOV(Ervebo)重组活疫苗的研发与试验,该疫苗在实地临床研究中显示接种者保护率接近100%,并最终于2019年获批使用。这一事件不仅造成严重公共卫生危机,也成为推动传染病诊断技术、抗病毒药物研发和全球卫生应急体系建设的转折点。
1.5防治对策
对策由于埃博拉病毒传播途径以体液接触为主(血液、呕吐物、尿液、汗液、精液等均可带毒),因此阻断传播链是核心策略。
病例隔离与接触者追踪:确诊和疑似病例需立即隔离,所有密切接触者进行21天医学观察,确保潜伏期内不遗漏传播源。
安全防护与防护用品:医护人员需使用符合标准的个人防护装备(PPE),包括防护服、手套、护目镜和N95口罩,避免在采血、护理、尸体处理过程中暴露。
安全埋葬:埃博拉患者遗体具有极高传染性,需采用安全埋葬措施,杜绝传统直接接触遗体的习俗。
健康教育与社区动员:向公众宣传埃博拉传播途径与预防措施,改变高风险行为(如食用野生动物、传统丧葬仪式),提升社区自我防控能力。
疫苗接种:目前WHO已推荐在高危人群中使用rVSV-ZEBOV(Ervebo)疫苗,在暴露前或暴露后环状接种均显示出近乎100%的保护效果。
目前尚无特效的广泛可及抗病毒药物,但近年来取得了突破性进展。
支持治疗:包括补液、电解质平衡、维持血压、输血和对症支持,是降低病死率的关键。改进的支持治疗使近期疫情病死率下降到约25-40%,明显低于早期的70-90%。
参考文献
[1] https://pubs.acs.org/doi/10.1021/acsnano.0c01739
[2] Reika Watanabe, Dawid Zyla, Diptiben Parekh et al. Intracellular Ebola virus nucleocapsid assembly revealed by in situ cryo-electron tomography, Cell, 2024, 187: 5587-5603.
[3] Fujita-Fujiharu Y, Hu S, Hirabayashi A et al. Structural basis for Ebola virus nucleocapsid assembly and function regulated by VP24. Nat Commun, 2025, 16: 2171.
[4] Rivera A, Messaoudi I. Molecular mechanisms of Ebola pathogenesis. J Leukoc Biol, 2016, 100: 889-904.
[5] Rojas M, Monsalve DM, Pacheco Y et al. Ebola virus disease: An emerging and re-emerging viral threat. J Autoimmun, 2020, 106: 102375.
[6] Jain S, Martynova E, Rizvanov A et al. Structural and Functional Aspects of Ebola Virus Proteins. Pathogens. 2021, 10: 1330.
[7] Martínez MJ, Biedenkopf N, Volchkova V et al. Role of Ebola virus VP30 in transcription reinitiation. J Virol, 2008, 82: 12569-73.
[8] Peng Q, Yuan B, Cheng J et al. Molecular mechanism of de novo replication by the Ebola virus polymerase. Nature, 2023, 622: 603-610.
.png)
