1.人类免疫缺陷病毒(Human immunodeficiency virus,HIV)
物种名:人类免疫缺陷病毒
拉丁学名:Human immunodeficiency virus (HIV)
分类学地位:病毒界Viruses;逆转录酶病毒门Artverviricota; 逆转录酶病毒纲Revtraviricetes;逆转录病毒目Ortervirales; 逆转录病毒科Retroviridae;慢病毒属Lentivirus
人类免疫缺陷病毒(Human Immunodeficiency Virus,HIV)是一种逆转录病毒,属于慢病毒科,主要通过血液、精液、阴道分泌液和母婴传播途径传播。HIV感染可导致人体免疫系统的逐渐破坏,最终引发获得性免疫缺陷综合症(AIDS)。HIV-1是全球最常见的毒株,而HIV-2则在西非地区较为普遍。HIV感染若不治疗,可导致免疫系统的严重衰弱,使机体易受各种机会性感染和某些类型癌症的侵害,严重威胁公共卫生。
1.1生物学特性
1.1.1培养特征
HIV作为一种逆转录病毒,其生活史极为复杂。当HIV感染人体,病毒表面的包膜糖蛋白gp120会与宿主细胞表面的CD4分子特异性结合,再借助辅助受体(如CCR5或CXCR4),促使病毒包膜与宿主细胞膜融合,病毒核心得以进入细胞内。在细胞内,病毒核心释放出两条单链RNA,在逆转录酶的作用下,以RNA为模板合成互补DNA(cDNA),这一过程即逆转录。随后,双链DNA进入细胞核,在整合酶协助下整合到宿主细胞基因组中,形成前病毒。前病毒可潜伏在宿主细胞内,随细胞分裂传递给子代细胞,免疫系统难以察觉。当宿主细胞被激活,前病毒转录形成RNA,部分RNA经修饰成为子代基因组RNA,另一些作为mRNA翻译出病毒蛋白。新合成的病毒蛋白和子代基因组RNA组装成新病毒颗粒,通过出芽方式从宿主细胞释放,继续感染其他细胞,循环感染过程[1]。
图1 HIV生命周期的简化表示[11]
1.1.2形态学特征
HIV病毒颗粒呈球形,直径约100–120 nm[2]。病毒由核心和包膜构成。包膜源于宿主细胞膜,镶嵌着由gp120和gp41组成的三聚体糖蛋白刺突。gp120位于包膜表面,负责识别并结合宿主细胞表面的CD4分子及辅助受体;gp41是跨膜蛋白,介导病毒包膜与宿主细胞膜的融合。包膜内是由p17蛋白构成的内膜。核心部分包含两条相同的正链RNA,被p24蛋白组成的衣壳包裹形成圆柱状核衣壳,核心内还存在逆转录酶、整合酶、蛋白酶和RNA酶H等对病毒复制至关重要的酶类[10]。
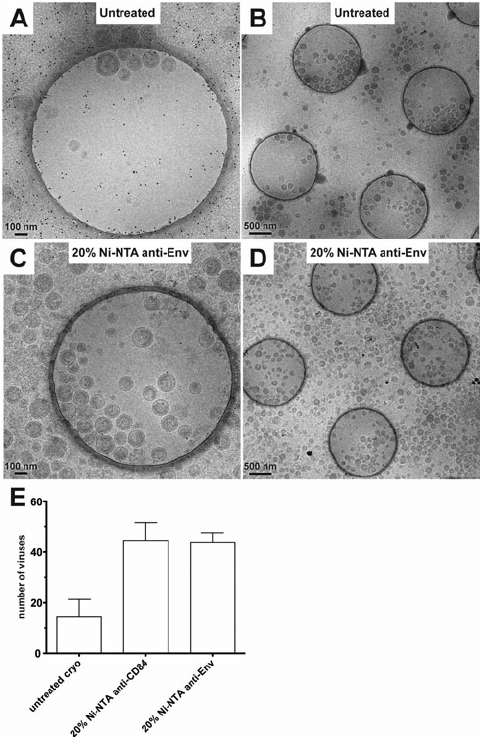
图2 人类免疫缺陷病毒(HIV)CD84病毒样颗粒(VLPs)[12]
A、B:应用于标准未处理的cryo-EM网格上的HIV CD84 VLPs的cryo-EM图像
1.1.3生化特征
从核酸层面看,HIV基因组由两条相同的单链RNA组成,携带多种蛋白的编码基因信息。gag基因编码核心蛋白,pol基因编码逆转录酶、整合酶和蛋白酶等,env基因编码包膜糖蛋白gp120和gp413。HIV的蛋白质功能多样,核心蛋白保护病毒基因组RNA,维持病毒颗粒结构稳定;逆转录酶以病毒RNA为模板合成cDNA,打破中心法则中遗传信息的转录方向;整合酶将病毒cDNA整合到宿主细胞基因组,使病毒长期潜伏;蛋白酶加工和成熟病毒蛋白,切割多聚蛋白为有活性的单个蛋白。此外,HIV包膜糖蛋白高度糖基化,影响病毒与宿主细胞的相互作用以及病毒的抗原性和免疫逃逸能力[10]。
1.1.4分子生物学特征
HIV的基因组RNA长约9.2 kb,前病毒DNA外侧附加LTR(长末端重复序列)序列后,长度变为9.8 kb。其基因结构复杂,有3个结构基因(gag、pol、env)和6个调节基因(tat、nef、vif、rev、vpr、vpu,HIV-2没有vpu,rpx基因)3。gag、pol、env、vpr、vpu、vif等编码的mRNA需REV蛋白协助胞质定位和表达,属于晚期基因;tat、nef等基因表达不依赖REV蛋白,为早期基因。HIV基因组变异频繁,同一感染者体内存在大量基因变异毒株,即准种。env基因编码的包膜糖蛋白变异最为频繁,突变率约1%,与流感病毒相似。env基因编码的gp120含与CD4分子和辅助受体结合位点,其变异决定HIV对淋巴细胞和巨噬细胞的亲嗜性,影响病毒中和抗原表位,给HIV疫苗研发带来巨大挑战[3]。
1.2分布、传播与致病性
1.2.1分布与传播
HIV携带者和艾滋病患者是唯一传染源[4]。从感染者的血液、精液、前列腺液、阴道分泌物、脑脊液、唾液、乳汁等标本中均可分离到HIV。其传播途径主要有性接触传播、血液传播和母婴传播。性接触传播是主要方式,包括同性、异性和双性性接触,HIV可通过性接触时的细微破损侵入机体,因精液中HIV含量远高于阴道分泌物,异性性接触中男性传给女性的概率相对较高。血液传播常见于共用针具静脉吸毒、输入被HIV污染的血液或血制品、介入性医疗操作等。母婴传播是感染HIV的孕妇经胎盘、分娩时通过产道、产后哺乳等将病毒传给婴儿。全球范围内,HIV感染分布广泛但地区差异大。截至2024年11月,全球约3990万人感染艾滋病病毒,非洲地区疫情最严重,撒哈拉以南非洲集中了全球约三分之二的HIV感染者。亚洲、美洲等地区也有不同程度感染,近年来亚洲部分国家HIV感染人数呈上升趋势[4]。
1.2.2致病性
HIV主要侵犯人体免疫系统,CD4+T淋巴细胞、巨噬细胞和树突状细胞是主要靶细胞,CD4+T淋巴细胞数量进行性减少是免疫功能缺陷的关键标志[5]。HIV感染人体后,病毒大量复制,一方面直接杀伤CD4+T淋巴细胞致其溶解破坏;另一方面诱导细胞凋亡,病毒复制中间产物、包膜糖蛋白gp120、调节蛋白vpr等均可诱导凋亡。gp120还可与未感染HIV的CD4+T细胞结合,使其成为靶细胞,遭受CD8+细胞毒性T细胞(CTL)介导的细胞毒作用及抗体依赖性细胞毒作用攻击,导致CD4+T细胞数量进一步减少。HIV感染还引起免疫系统异常激活,CD4+、CD8+T细胞表达CD69、CD38和HLA-DR等免疫激活标志物水平异常升高,且与HIV血浆病毒载量相关,疾病进展时免疫异常激活水平上升。免疫系统受损后,患者易出现各种机会性感染和肿瘤,如肺孢子菌肺炎、隐球菌脑膜炎、白色念珠菌食管炎、结核杆菌感染、卡波西肉瘤、非霍奇金淋巴瘤等[5]。
1.3检测方法
HIV检测对疾病诊断、治疗和防控意义重大。常用检测方法有抗体检测、抗原检测、核酸检测和耐药检测等[6]。抗体检测是诊断金标准,采用ELISA、化学发光法或免疫荧光法初筛和复检血清中的gp24及gp120抗体,灵敏度达99%,初筛结果需经蛋白印迹(Western blot,WB)检测确认。但HIV感染有窗口期,此期间抗体可能未产生,抗体检测存在局限性。抗原检测主要测抗HIV p24抗原,有助于抗体产生窗口期和新生儿早期感染诊断,常用ELISA法测血清HIV p24抗原。核酸检测可测定病毒载量,用于了解疾病进展、提供抗病毒治疗依据、评估治疗效果、指导治疗方案调整及早期诊断,常用方法有反转录PCR、核酸序列依赖性扩增、分枝DNA信号放大系统和实时荧光定量PCR扩增等。耐药检测通过测定HIV基因型和表型变异了解药物变异情况,国内外主要采用基因型检测,一般在抗病毒治疗病毒载量下降不理想或治疗失败需改变治疗方案时进行,条件允许时也可在治疗前进行,有助于选择合适抗病毒药物[7]。
1.4典型案例
1981年,美国疾病控制与预防中心首次报告5例罕见的卡氏肺孢子虫肺炎病例,患者均为男同性恋者,拉开艾滋病大流行序幕[8]。随后更多类似病例出现,患者伴有免疫系统严重受损表现。1983年,法国病毒学家Luc Montagnier和Francoise Barre-Sinoussi等成功分离出HIV病毒,明确艾滋病病原体[1]。疫情初期,因对疾病认识不足,在男同性恋、静脉注射毒品者等高危人群中迅速传播。如20世纪80年代美国,艾滋病在纽约、旧金山等大城市男同性恋社区蔓延,许多患者因未及时诊断和治疗死亡,冲击社会[9]。2024年2月,68岁的美国加州男子保罗·埃德蒙经骨髓移植5年后,急性髓性白血病基本治愈,成为全球第5个艾滋病被治愈的人,为艾滋病治愈研究带来新希望,表明特定条件下艾滋病有可能被攻克。
1.5防治对策
因目前无有效HIV疫苗,预防主要依靠综合措施[4]。加强健康教育,提高公众对HIV传播途径、危害及预防方法的认识,倡导安全性行为,正确使用安全套,避免不必要注射和输血等高危行为,保持健康生活方式,可降低感染风险。对于高危人群,如男男同性性行为者、静脉注射毒品者、多性伴人群等,可采用暴露前预防(PrEP)措施,服用抗逆转录病毒药物降低感染风险。治疗方面,抗逆转录病毒治疗(ART)是主要方法,通过联合使用抑制逆转录酶、蛋白酶、病毒进入细胞、整合酶等类型的药物,最大限度抑制病毒复制,恢复和维持免疫功能,降低艾滋病相关疾病发病率和死亡率,提高患者生活质量[6]。发生HIV暴露,无论是职业暴露(如医务人员被HIV污染针头刺伤)还是非职业暴露(如高危性行为后),应立即评估,尽快(最好2小时内)进行预防性用药,并在暴露后立即、4周、8周、12周和6月后检测HIV抗体,监测是否感染[9]。
参考文献
[1] Barré-Sinoussi F, Chermann JC, Rey F, Nugeyre MT et al. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS). Science, 1983, 220: 868-71.
[2] Ganser-Pornillos BK, Yeager M, Pornillos O. Assembly and architecture of HIV. Adv Exp Med Biol, 2012, 726: 441-65.
[3] Miura T, Brockman MA, Brumme CJ et al. Genetic characterization of human immunodeficiency virus type 1 in elite controllers: lack of gross genetic defects or common amino acid changes. J Virol, 2008, 82: 8422-30.
[4] https://www.who.int/news-room/fact-sheets/detail/hiv-aids
[5] Baeten JM, Chohan B, Lavreys L et al. HIV-1 subtype D infection is associated with faster disease progression than subtype A in spite of similar plasma HIV-1 loads. J Infect Dis, 2007, 195: 1177-80.
[6] https://clinicalinfo.hiv.gov/sites/default/files/guidelines/documents/adult-adolescent-arv/guidelines-adult-adolescent-arv.pdf#:~:text=Panel%20on%20Antiretroviral%20Guidelines%20for%20Adults%20and%20Adolescents.,of%20Health%20and%20Human%20Services.%20Available%20at%20https%3A%2F%2Fclinicalinfo.hiv.gov%2Fen%2Fguidelines%2Fadult-and-adolescent-arv.
[7] Consolidated guidelines on differentiated HIV testing services [Internet]. Geneva: World Health Organization, 2024.
[8] Gottlieb MS, Schroff R, Schanker HM et al. Pneumocystis carinii pneumonia and mucosal candidiasis in previously healthy homosexual men: evidence of a new acquired cellular immunodeficiency. N Engl J Med, 1981, 305: 1425-31.
[9] https://www.cdc.gov/museum/online/story-of-cdc/aids/index.html.
[10] Fuller SD, Wilk T, Gowen BE et al. Cryo-electron microscopy reveals ordered domains in the immature HIV-1 particle. Curr Biol, 1997, 7: 729-38.
[12] Kiss G, Chen X, Brindley MA et al. Capturing enveloped viruses on affinity grids for downstream cryo-electron microscopy applications. Microsc Microanal, 2014, 20: 164-74.
.png)
