1.柔嫩艾美耳球虫(Eimeria tenella)
物种名:柔嫩艾美耳球虫
拉丁学名:Eimeria tenella
分类学地位: 真核生物域Eukaryota;顶复门Apicomplexa;锥体纲Conoidasida;球虫亚纲Coccidiasina;艾美耳目Eimeriida;艾美耳科Eimeriidae;艾美耳属EimeriaCandida
柔嫩艾美耳球虫是一种单细胞的专性细胞内寄生原虫,是引起鸡盲肠球虫病的病原体。该寄生虫具有高度的宿主特异性,主要感染鸡,不感染人类。它是全球家禽业最具致病性和经济破坏性的寄生虫之一,感染可导致鸡群出现严重的血便、高死亡率和生产性能下降,给集约化养鸡业带来巨大的经济损失[1]。
1.1生物学特性
1.1.1培养特征
柔嫩艾美耳球虫是专性细胞内寄生虫,无法在常规的无细胞人工培养基上生长。其“培养”或繁殖依赖于活体宿主(鸡)或体外细胞培养系统,整个过程即为其完整的生活史。
(1)体外阶段(孢子化):鸡排出未孢子化的卵囊(如图1所示),其不具感染性。在外界有适宜温度(21-32℃)、湿度和氧气的条件下,经过1-2天发育,形成含有4个孢子囊、每个孢子囊内含2个子孢子的感染性卵囊。
(2)体内阶段:鸡摄入感染性卵囊后,卵囊在消化道内脱囊,释放出子孢子。子孢子特异性地侵入盲肠上皮细胞,进行两代裂殖生殖(无性繁殖),产生大量裂殖子,导致宿主细胞大量破裂和严重出血。随后,裂殖子发育成雌、雄配子,通过有性生殖形成合子,最后发育成新的卵囊随粪便排出体外[1]。整个体内发育周期约7天[2]。
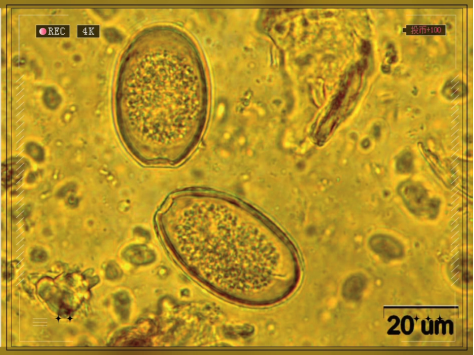
图1 柔嫩艾美耳球虫卵囊
1.1.2形态学特征
诊断主要依据其卵囊形态。卵囊呈宽卵圆形,大小约为19-26 µm×16-22 µm,有一个小的极体,但无残体和卵黄体。囊壁光滑,呈双层。孢子化卵囊内含4个孢子囊,每个孢子囊内含2个子孢子。柔嫩艾美耳球虫引起的病理变化极具特征性,主要表现为盲肠肿胀、增厚,内容物为凝固的血液或血块(图2)[3]。
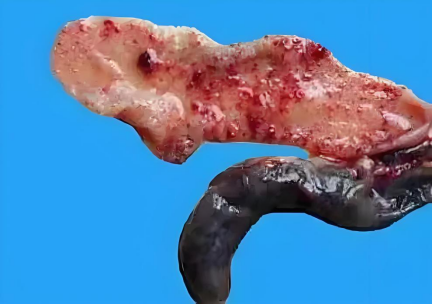
图2 球虫病病变病理图
1.1.3生化特征
作为专性细胞内寄生虫,其生化特征主要体现在其独特的代谢方式和与宿主的相互作用上。柔嫩艾美耳球虫在细胞内阶段主要依赖糖酵解途径获取能量,即使在有氧环境下也倾向于产生大量乳酸,这是一种类似于“瓦博格效应”的代谢特征。其拥有高效的乳酸脱氢酶(LDH)。在入侵宿主细胞时,其顶复器(如微线体、棒状体)会分泌多种水解酶,如半胱氨酸蛋白酶等,用于降解宿主细胞外基质和细胞膜,从而顺利侵入[4]。
1.1.4分子生物学特征
柔嫩艾美耳球虫的致病机制与其在宿主细胞内的快速增殖和诱导强烈的炎症反应有关。其顶复器(含有棒状体、微线体等)分泌的蛋白在入侵宿主细胞过程中起关键作用。分子鉴定主要依赖于物种间差异显著的基因序列,如内转录间隔区(ITS-1, ITS-2)和线粒体细胞色素c氧化酶亚基I(COI)基因,这些序列是开发物种特异性PCR诊断方法的基础[5]。
1.2分布、传播与致病性
1.2.1分布与传播
该寄生虫呈世界性分布,存在于所有养鸡的国家和地区。传播途径为典型的粪-口途径。受感染的鸡通过粪便排出大量卵囊,污染垫料、饲料、饮水和设备。健康的鸡通过啄食被感染性卵囊污染的物质而感染。卵囊抵抗力强,能在环境中存活数月之久。
1.2.2致病性
柔嫩艾美耳球虫是致病力最强的鸡球虫之一。主要侵害4-8周龄的雏鸡和青年鸡。临床表现为精神沉郁、羽毛松乱、食欲废绝、最终排出特征性的鲜红色血便。严重感染时,鸡只因大量失血和继发感染,死亡率可高达80%以上。幸存的鸡也生长受阻,成为僵鸡。感染剂量较低,摄入1000个左右的感染性卵囊即可引起临床症状[2]。
其不属于人类病原体,因此不适用于人类生物安全等级(BSL)划分。它是一种重要的兽医病原体。作为禽类寄生虫,在任何人类饮用水或地表水标准(如GB5749, GB3838)中均没有相关限值规定。在养殖业中,其控制标准主要体现在鸡粪或垫料样品中每克卵囊数(Oocysts Per Gram, OPG)。OPG是评估鸡群感染压力和判断是否需要采取干预措施的重要指标,但没有统一的法定阈值,通常由兽医根据具体情况判断。
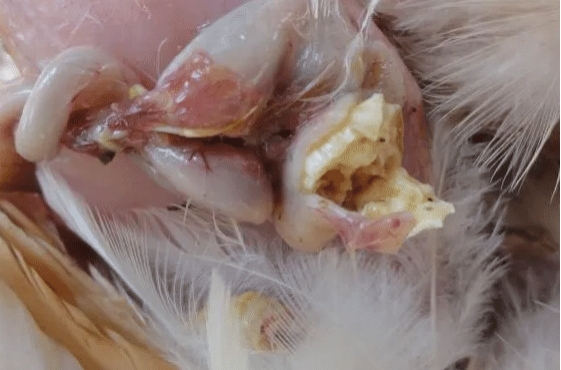
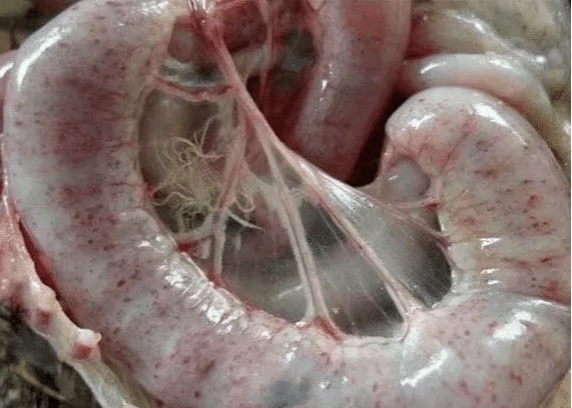
图3 禽类感染球虫病下的柔嫩艾美耳球虫
1.3检测方法
(1)盲肠病变评分与粪便卵囊计数法:这是兽医临床和研究中诊断球虫病的经典和标准方法。其操作原理分为病变评分和卵囊计数。病变评分:对可疑病死鸡进行剖检,观察盲肠的病理变化(出血、肿胀、内容物等),并根据国际通用的Johnson和Reid病变评分法进行0-4级的半定量评分,4分代表最严重病变和死亡。卵囊计数:收集粪便或垫料样本,采用饱和盐水漂浮法和麦克马斯特计数板(McMaster slide)在显微镜下对卵囊进行计数,计算出OPG值。该方法是中国农业行业标准《鸡球虫病诊断技术》(NY/T 1460-2007)中规定的核心诊断技术[6]。
(2)物种特异性PCR法:该方法用于精确鉴定引起病变的球虫种类,对制定精准防控方案至关重要。其操作原理为从粪便或盲肠组织中提取总DNA,利用针对柔嫩艾美耳球虫特异性基因序列(通常是ITS-1区)设计的引物进行PCR扩增。通过琼脂糖凝胶电泳检测有无预期大小的特异性条带,来判断样本中是否存在柔嫩艾美耳球虫。其常用引物(ITS-1区)如表1,预期产物大小约298 bp。该引物对在多种研究中被证明具有良好的物种特异性,其方法和应用可见于相关兽医寄生虫学文献[5]。
表1 柔嫩艾美耳球虫PCR法ITS-1区常用引物序列
| 名称 | 序列 |
| ET-F(正向) | 5′-TGACCGCCGAGAAGAGCAA-3′ |
| ET-R(反向) | 5′-CTCTTCTTCGTCCATCGCCTC-3′ |
1.4典型案例
在一个存栏量为10万只的大型肉鸡场,一批饲养至28日龄的肉鸡突然出现大规模发病。鸡群表现为精神萎靡、采食量急剧下降、羽毛蓬乱,并排出大量鲜红色血便。在短短三天内,死亡率从不足0.1%飙升至15%,造成了巨大的经济损失。兽医现场剖检发现,病死鸡盲肠极度肿胀,呈暗红色,肠腔内充满凝固的血块,盲肠病变评分均达到4分。实验室通过饱和盐水漂浮法对粪便进行卵囊计数,测得OPG值高达5.0×105,远超警戒水平。为进一步确诊,对盲肠组织进行PCR检测,结果显示柔嫩艾美耳球虫ITS-1基因为强阳性。调查发现,此次暴发是由于该批次饲料中添加的抗球虫药(如地克珠利)已产生严重耐药性,且近期阴雨天气导致垫料潮湿,为卵囊的孢子化创造了有利条件。养殖场立即对全场鸡只通过饮水投喂妥曲珠利进行紧急治疗,并对重污染区的垫料进行更换和火焰消毒,同时加强通风,最终控制了疫情。该事件导致该场直接经济损失超过50万元,并促使该企业重新评估其球虫病防控策略,决定在后续批次中采用疫苗进行免疫预防[7]。
1.5防治对策
(1)药物预防与治疗:在饲料或饮水中添加抗球虫药是目前最主要的控制手段。为延缓耐药性,常采用“穿梭用药”(不同生长阶段使用不同药物)和“轮换用药”(不同批次使用不同药物)策略。
(2)免疫预防:使用球虫病活疫苗(含致弱或非致弱的感染性卵囊)是建立鸡群主动免疫、实现可持续控制的有效方法,尤其适用于种鸡和蛋鸡。
(3)饲养管理与生物安全:保持禽舍干燥、通风,是抑制卵囊孢子化的关键。实行“全进全出”的饲养制度,在每批鸡出栏后,对禽舍和设备进行彻底的清洁和消毒(如使用氨水熏蒸或火焰消毒),能有效清除环境中的卵囊,切断传播链[1]。
参考文献
[1] 苏瑞, 韩红玉, 董辉 等. 鸡球虫病研究进展. 中国动物传染病学报, 2021, 29: 93-102.
[2] 陈福勇, 王海东, 郝拉娣 等. 鸡柔嫩艾美耳球虫的生物学特性及其防治研究进展. 动物医学进展, 2011, 32: 86-90.
[3] 赵俊龙, 张西西, 董晓晴 等. 鸡柔嫩艾美耳球虫山西分离株的分离鉴定及致病性研究. 中国兽医杂志, 2023, 59: 10-14.
[4] 李赫, 赵巧玲, 王梦雅 等. 柔嫩艾美耳球虫乳酸脱氢酶的分子特征与功能分析. 中国兽医学报, 2015, 35: 1342-1348.
[5] 付钰, 李建华, 李祥瑞 等. 鸡7种艾美耳球虫ITS-1序列多重PCR鉴别方法的建立与应用. 中国兽医学报, 2012, 32: 1538-1543.
[6] 中华人民共和国农业部. NY/T 1460-2007 鸡球虫病诊断技术. 北京: 中国农业出版社, 2007.
[7] 崔杏站, 吴孔菊, 韩子帅 等. 一起肉鸡柔嫩艾美耳球虫病的诊治. 养禽与禽病防治, 2021: 54-55.
.png)
