1.沙眼衣原体(Chlamydia trachomatis)
物种名:沙眼衣原体
拉丁学名:Chlamydia trachomatis
分类学地位:细菌界Bacteria;衣原体门Chlamydiota;衣原体纲Chlamydiia; 衣原体目Chlamydiales;衣原体科Chlamydiaceae; 衣原体属Chlamydia
沙眼衣原体(Chlamydia trachomatis)是一种专性细胞内寄生的革兰氏阴性细菌,为衣原体属的重要病原菌。该菌主要通过性接触或母婴传播,可引起人类泌尿生殖道感染、沙眼及包涵体结膜炎等疾病。其中,血清型A-C主要引起沙眼,是全球可预防性失明的主要感染因素之一;D-K型则与泌尿生殖道感染密切相关,可导致非淋菌性尿道炎、宫颈炎、盆腔炎,甚至不孕不育。近年来,沙眼衣原体感染已成为全球范围内重要的公共卫生问题[1]。
1.1生物学特性
1.1.1培养特征
沙眼衣原体为专性细胞内寄生原核生物,不能通过体外无细胞培养基培养,必须依赖宿主细胞进行复制。常用McCoy细胞、HeLa-229细胞或BHK-21细胞等哺乳动物细胞系进行分离培养。在细胞内,沙眼衣原体以独特的发育周期增殖,形成典型的包涵体(inclusion bodies)(图1),包涵体多位于细胞核旁,早期呈致密颗粒状,随感染进展逐渐增大,可被碘液染色以及荧光染料染色。由于其无法在常规琼脂平板上生长,因此不形成传统意义上的菌落。在鸡胚卵黄囊接种或细胞培养中,可观察到细胞病变效应(CPE),表现为细胞圆缩、脱落等。部分血清型(如D-K型)在泌尿道上皮细胞中感染后可引起慢性炎症反应,但不产生溶血现象[2]。
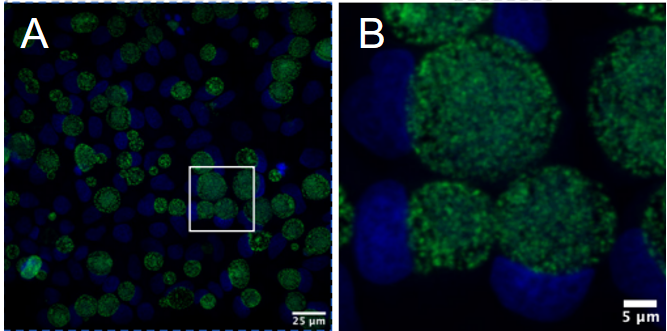
图1 沙眼衣原体荧光染色结果[16]
1.1.2形态学特征
沙眼衣原体为革兰氏阴性菌,染色后呈红色,菌体微小,直径约0.2-0.3 μm。存在两种形态:感染性的原体(EB)和繁殖性的始体(RB)。无鞭毛,不具运动能力,不形成芽孢。专性细胞内寄生,在宿主细胞内增殖并形成包涵体,是其重要的形态学标志[3]。
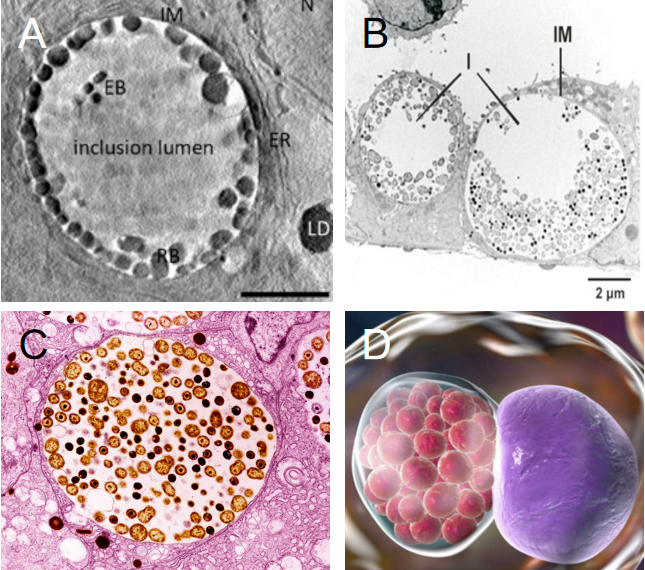
图2 沙眼衣原体显微照片
A:冷冻电镜照片[17],B:扫描电镜照片[18]
C:透射电镜照片[18],D:三维成像[19]
1.1.3生化特征
沙眼衣原体为专性细胞内寄生菌,无独立代谢能力,不能在无细胞培养基中生长,不发酵糖类,不产酸、不产气,不液化明胶,不分解尿素,不产生硫化氢,V-P试验和M.R试验均阴性。其能量代谢依赖宿主细胞,通过摄取宿主ATP进行生物合成,故对影响宿主代谢或蛋白质合成的抗生素敏感,如四环素类、大环内酯类,但对作用于细胞壁的抗生素(如青霉素)不敏感[4]。由于缺乏典型生化反应特性,其鉴定主要依赖分子生物学方法或免疫学检测[5]。
1.1.4分子生物学特征
沙眼衣原体基因组为单条环状双链DNA,大小约1.04-1.23 Mb,GC含量约41%-44%,含有约900-1100个潜在编码序列,已明确功能的基因约600个。基因组中存在多个与毒力相关的基因,如编码主要外膜蛋白(Major Outer Membrane Protein, MOMP)的ompA基因,该基因是血清分型的主要依据,不同血清型ompA基因序列存在差异;还有编码热休克蛋白(Heat Shock Protein, HSP)的hsp60基因,与衣原体的黏附、入侵及免疫致病相关[6]。此外,沙眼衣原体不含质粒,其基因表达调控主要依赖启动子区域的调控序列及转录因子,部分基因的表达具有发育周期特异性,如原体阶段主要表达与感染相关的基因,始体阶段主要表达与繁殖相关的基因[7]。
1.2分布、传播与致病性
1.2.1分布与传播
沙眼衣原体主要寄生于人的眼结膜和泌尿生殖道黏膜上皮细胞,不能在外界环境中自主繁殖。其在水环境中的分布虽不具增殖能力,但感染者的眼部分泌物可污染水源,如洗脸水、井水、池塘或共用洗浴设施,原体在阴暗潮湿的水体中可保持感染性数小时至数天,成为儿童沙眼传播的重要途径。在卫生条件差的地区,共用污染水源或毛巾极易造成家庭和社区内传播。苍蝇亦可机械性携带病原体扩散。D-K型和L型主要通过性接触传播,母婴垂直传播则发生在分娩过程中,新生儿经产道接触感染分泌物可致结膜炎和肺炎。感染全年均可发生,高发于卫生落后地区的儿童、育龄妇女及新生儿[8]。
1.2.2致病性
沙眼衣原体是一种专性细胞内寄生的病原体,其致病性依赖于独特的双相发育周期和对宿主细胞的侵袭能力。感染初期,具有高度感染性的原体(Elementary Body, EB)通过主要外膜蛋白(MOMP)和黏附素与宿主细胞表面受体结合,介导内吞进入细胞。进入细胞后,原体在细胞质内形成包涵体,并转化为代谢活跃但无感染性的始体(Reticulate Body, RB),利用宿主提供的ATP进行二分裂增殖。后期始体重新转化为原体,最终导致宿主细胞破裂,释放出大量子代原体,感染邻近细胞,引发局部炎症和组织损伤。持续或反复感染可导致慢性炎症和纤维化,是其致病的关键机制[9]。
沙眼衣原体根据血清型不同可分为多个致病类群,其中A-C型主要引起沙眼,D-K型引起泌尿生殖道感染,L1-L3型则导致性病淋巴肉芽肿(LGV)。其致病效力由多种毒力因子共同决定,包括主要外膜蛋白(MOMP)、脂多糖(LPS)、III型分泌系统(T3SS)效应蛋白和热休克蛋白(HSP60)等。MOMP是外膜的主要结构蛋白,参与黏附宿主细胞并具有血清型特异性;LPS可激活宿主免疫系统,引发强烈的炎症反应;T3SS则像“分子注射器”,将效应蛋白注入宿主细胞,抑制溶酶体融合、干扰细胞凋亡和免疫识别,帮助衣原体在细胞内存活和复制。HSP60在持续感染中大量表达,可诱发自身免疫反应,导致组织瘢痕形成,如输卵管阻塞、角膜混浊等[10]。
沙眼衣原体感染后可引起多种疾病:A-C型感染眼结膜,表现为滤泡性结膜炎,反复感染可导致睑内翻、倒睫、角膜血管翳,最终造成不可逆性失明,是全球可预防性盲症的首要原因;D-K型侵犯泌尿生殖道,男性可引起非淋菌性尿道炎、附睾炎,女性则表现为宫颈炎、尿道炎,若上行感染可导致盆腔炎、不孕或异位妊娠;L1-L3型引起性病淋巴肉芽肿,表现为生殖器初疮、腹股沟淋巴结肿痛及直肠狭窄。此外,新生儿经产道感染可发生包涵体性结膜炎和衣原体肺炎。感染后还可能诱发反应性关节炎,表现为关节炎、尿道炎和结膜炎三联征。根据致病部位和机制,沙眼衣原体所致疾病分类见表3[11]。
表1 致病性沙眼衣原体分类及相应疾病[10]
| 沙眼衣原体致病类型 | 疾病 |
| 眼部致病性沙眼衣原体 | |
| 1.包涵体结膜炎生物型 | 新生儿和成人包涵体结膜炎 |
| 2.沙眼生物型 | 儿童水样腹泻 |
| 泌尿生殖系统致病性沙眼衣原体 | |
| 1.沙眼生物型 | 持续性水样腹泻 |
| 2.性病淋巴肉芽肿生物型 | 急性水样腹泻 |
1.3检测方法
- 传统方法:沙眼衣原体的检测方法多样,传统技术主要包括细胞培养、直接显微镜检查和抗原检测。细胞培养曾被视为诊断“金标准”,通过在McCoy或HeLa细胞系中培养临床样本,观察包涵体形成,并结合Giemsa或荧光抗体染色进行鉴定。该方法特异性高,但操作复杂、耗时长(48-72小时)、对样本运输和保存条件要求高,已逐渐被分子方法取代。直接显微镜检查包括Giemsa染色和碘染色,适用于新生儿结膜刮片,可观察细胞内包涵体,但灵敏度较低。免疫学检测方法如酶联免疫吸附试验(ELISA)和直接荧光抗体检测(DFA)可用于检测衣原体抗原,具有较高特异性,且灵敏度优于ELISA,是较常用的抗原检测手段[12]。
(2)新型检测法:目前最常用且最敏感的方法是核酸扩增检测(NAATs),包括实时荧光PCR、转录介导扩增(TMA)和链置换扩增(SDA)。
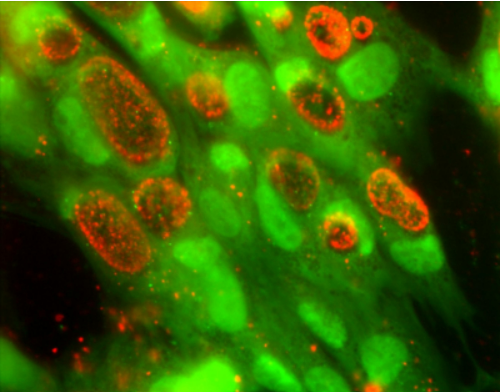
图4 免疫荧光法检测沙眼衣原体[20]
1.4典型案例
2020年7月,西部某县农村地区发生沙眼集中流行:当地集中供水工程的水源井因雨水倒灌被生活污水污染,水中检出沙眼衣原体(A、C血清型)。此次流行共波及3个行政村,累计报告沙眼病例157例,患者均出现结膜充血、滤泡增生等症状,其中21名未及时治疗的儿童发展为慢性沙眼,出现角膜血管翳,需长期随访治疗。当地政府紧急启动应急供水方案,对水源地进行净化消毒,并为村民开展免费筛查治疗,直接经济投入达180万元。
2022年6月,美国得克萨斯州休斯顿市某社区公共泳池爆发沙眼衣原体感染疫情:经疾控中心(CDC)溯源,该泳池因管道老化导致消毒水分布不均,池水中检出沙眼衣原体(D、E血清型),污染源为一名无症状带菌者的排泄物污染。疫情持续2周,共报告103例感染病例,其中78人确诊为包涵体结膜炎,12名男性出现尿道炎症状。泳池被迫关闭10天进行系统改造与消毒,相关费用及医疗支出合计超40万美元,还被州卫生部门处以12万美元罚款[12]。
1.5防治对策
防控沙眼衣原体需抓关键环节:做好粪便处理防水源污染,定期检测水源并规范消毒饮用水;管控泳池等场所,确保水循环消毒合格;及时用阿奇霉素等治疗感染者及密切接触者,消毒污染物品;卫生部门开展宣教、筛查,推广快速检测以早发现早治。
参考文献
[1] WHO. Global report on neglected tropical diseases 2023: Ending the neglect of poverty-related infections. Geneva: World Health Organization, 2023.
[2] Wang SP, Grayston JT. Microbiological examination of ocular chlamydial isolates. Investigative Ophthalmology & Visual Science, 1975, 14: 57-65.
[3] Phillips P, Parkhurst JM, Kounatidis I, et al. Single cell cryo-soft X-ray tomography shows that each Chlamydia trachomatis inclusion is a unique community of bacteria . Life, 2021, 11: 842.
[4] Beatty WL, Byrne GI, Morrison RP. Repeated stimulation by Chlamydia outer membrane protein (OmpA) causes macrophage apoptosis . Infection and Immunity, 1994, 62: 3727-3735.
[5] Hammerschlag MR. Azithromycin: its role in the treatment of Chlamydia trachomatis infections. Expert Opinion on Pharmacotherapy, 2001, 2: 209-217.
[6] Stephens RS, Kalman S, Lammel C, et al. Genome sequence of an obligate intracellular pathogen Chlamydia trachomatis. Science, 1998, 282: 754-759.
[7] Zhang YX, Stewart S, Seto D, et al. Structure, alignment, evolution, and analysis of amplified sequences within the three-variable domains of Chlamydia trachomatis serovar-specific epitope. Infection and Immunity, 1987, 55: 1527-1535.
[8] Burton MJ, Bowman RJ, Faal H, et al. Persistent hyperendemic trachoma in a very hot and dry setting: implications for elimination. PLoS Neglected Tropical Diseases, 2009, 3: e526.
[9] Zhong G. Chlamydia persistence: beyond the biphasic paradigm. Infection and Immunity, 2009, 77: 827-833.
[10] Morré SA, vanValkengoed I, Moes R, et al. The heat shock protein 60 (hsp60) homologue in Chlamydia spp. is associated with the persistence of the organism. Microbes and Infection, 2002, 4: 761-767.
[11] Peeling R W, Mabey D. Point-of-care tests for diagnosing Trachoma and other neglected tropical diseases. Expert Review of Molecular Diagnostics, 2010, 10: 413-421.
[12] 李婷, 张丽, 王强. 沙眼衣原体核酸检测技术研究进展. 中华检验医学杂志, 2022, 45: 298-303.
[13] 赵敏, 刘芳, 陈军. 沙眼衣原体感染的流行病学特征及防治策略. 中国公共卫生, 2021, 37: 721-724.
[14] 孙伟, 周琳, 吴雪. 核酸扩增技术在沙眼衣原体检测中的应用评价. 国际检验医学杂志, 2023, 44: 189-193.
[15] 黄静, 李红, 郑晓霞. 沙眼衣原体血清型分布与耐药性监测. 中国抗生素杂志, 2020, 45: 745-749.
[16] 王磊, 杨帆, 赵静. 沙眼衣原体致不孕机制研究进展. 中华妇产科杂志, 2021, 56: 501-505.
[17] hillips P, Parkhurst JM, Kounatidis I, Okolo C, Fish TM, Naismith JH, Walsh MA, Harkiolaki M, Dumoux M. Single Cell Cryo-Soft X-ray Tomography Shows That Each Chlamydia Trachomatis Inclusion Is a Unique Community of Bacteria. Life, 2021, 11: 842.
[18] https://www.researchgate.net/publication/46770842 Global assessment of host cell functions involved in the intracellular survival and replication of Chlamydia using RNA interference in human cells.
[19] https://phil.cdc.gov/QuickSearch.aspx?key=true
[20] Singla M, Bal B. Infectivity Assays For Chlamydia Trachomatis. The Internet Journal of Microbiology, 2005 , 2: 2.
.png)
