1.问号钩端螺旋体(Leptospira interrogans)
物种名:问号钩端螺旋体
拉丁学名:Leptospira interrogans
分类学地位: 细菌界Bacteria;螺旋体门Spirochaetota;
螺旋体纲Spirochaetia;螺旋体目Spirochaetales;
钩端螺旋体科Leptospiraceae;钩端螺旋体属Leptospira
问号钩端螺旋体(Leptospira interrogans)是一种广泛分布于全球水体和土壤中的病原性螺旋体,可通过接触受感染动物的尿液或污染的水源传播给人类和动物,引起钩端螺旋体病(Leptospirosis)。该病是一种重要的人畜共患病,尤其在热带和亚热带地区流行严重。
1.1生物学特性
1.1.1培养特征
问号钩端螺旋体为专性需氧菌,最适生长温度为28-30℃,最适pH为7.2-7.6。可在含有10%兔血清的EMJH培养基上生长,形成透明、扁平、边缘不规则的菌落。生长缓慢,通常需培养1-2周方可观察明显生长。
1.1.2形态学特征
c
b
问号钩端螺旋体呈细长、螺旋状,长约6-20 μm,直径约0.1 μm,具有内鞭毛(endoflagella),运动活泼,呈旋转或蛇形前进。革兰氏染色阴性,但不易着色,常用镀银染色(如Fontana染色)或暗视野显微镜观察(图1)[1]。
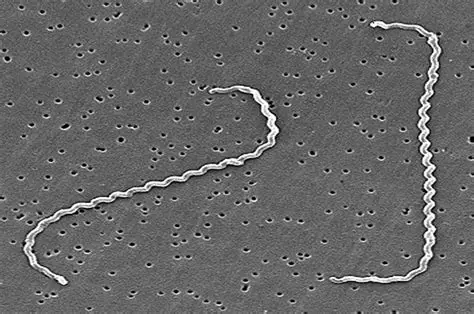
图1 问号钩端螺旋体暗视野显微镜下形态(×1000)[2]
1.1.3生化特征
问号钩端螺旋体不能发酵糖类,不产生吲哚,不还原硝酸盐,氧化酶和过氧化氢酶阳性。能利用长链脂肪酸作为碳源和能源。对某些抗生素如青霉素、多西环素敏感,但对磺胺类药物耐药[3]。
1.1.4分子生物学特征
问号钩端螺旋体基因组大小约为4.6 Mbp,包含约4700个基因。其基因组中包括多个编码外膜蛋白(如LipL32、LipL41、OmpL1)的基因,这些蛋白在致病性和免疫应答中起关键作用。此外,还含有多个与运动、趋化和宿主互作相关的基因[4]。
1.2分布、传播与致病性
1.2.1分布与传播
问号钩端螺旋体广泛分布于温暖潮湿的地区,尤其是热带和亚热带的河流、湖泊、稻田和沼泽地。主要通过接触受感染动物(如鼠类、猪、狗等)的尿液或污染的水源、土壤传播给人类。人群普遍易感,农民、渔民、下水道工人等职业人群感染风险较高[5]。
1.2.2致病性
问号钩端螺旋体可引起人类钩端螺旋体病,临床表现多样,从轻微发热、头痛、肌肉痛到严重的威尔氏病(Weil’s disease),表现为黄疸、出血倾向、肾功能衰竭等。其致病机制与细菌的黏附、侵袭、毒素产生及免疫逃避有关。主要毒力因子包括外膜蛋白、溶血素、脂多糖(LPS)等[6]。
1.3检测方法
(1)微生物培养法:采集患者血液、尿液或脑脊液,接种于EMJH培养基,28-30℃培养1-4周,通过暗视野显微镜观察确认。
(2)血清学检测:常用显微镜凝集试验(MAT)检测特异性抗体,也可采用ELISA、免疫荧光等方法。
(3)分子生物学方法:PCR检测特异性基因(如1lipL32),具有快速、灵敏、特异性高等优点[7]。
1.4典型案例
2017年,斯里兰卡因暴雨洪水爆发大规模钩端螺旋体病疫情,报告病例超过3000例,多数患者为洪水接触者。研究表明,洪水导致鼠类尿液广泛污染水源,是疫情暴发的主要原因[8]。
2020年,巴西一项研究发现,城市贫民窟中的鼠类携带多种致病性钩端螺旋体血清型,居民感染率显著高于其他地区,提示环境卫生差和鼠类控制不力是疫情持续的重要因素[9]。
1.5防治对策
预防钩端螺旋体病的关键在于避免接触可能被污染的水源和动物尿液,加强个人防护(如穿防水靴、手套),改善环境卫生,控制鼠类等宿主动物。疫苗主要用于家畜和高风险职业人群,人类疫苗仍在研发中。治疗首选抗生素如青霉素、多西环素,早期治疗效果好[10]。
参考文献
[1] Levett PN. Leptospirosis. Clin Microbiol Rev, 2001, 14: 296-326.
[2] Picardeau M. Virulence of the zoonotic agent of leptospirosis: still terra incognita Nat Rev Microbiol, 2017, 15: 297-307.
[3] Haake DA, Levett PN. Leptospirosis in humans. Curr Top Microbiol Immunol, 2015, 387: 65-97.
[4] Nascimento ALTO. The genome of Leptospira interrogans serovar Copenhageni reveals unexpected metabolic capabilities. Proc Natl Acad Sci USA, 2004, 101: 3136-3141.
[5] Costa F. Global morbidity and mortality of leptospirosis: a systematic review. PLoS Negl Trop Dis, 2015, 9: e0003898.
[6] Murray GL. The molecular basis of leptospiral pathogenesis. Curr Top Microbiol Immunol, 2015, 387: 139-185.
[7] Ahmed A. Development and validation of a real-time PCR for detection of pathogenic Leptospira species in clinical materials. PLoS One, 2009, 4: e7093.
[8] Agampodi SB. Leptospirosis outbreak in Sri Lanka in 2017: lessons learned and future directions. Lancet Infect Dis, 2018, 18: e128-e133.
[9] Reis RB. Impact of environment and social gradient on Leptospira infection in urban slums. PLoS Negl Trop Dis, 2020, 14: e0008127.
[10] WHO. Human leptospirosis: guidance for diagnosis, surveillance and control. Geneva: World Health Organization, 2003.
.png)
