1.曲霉菌属(Aspergillus)
物种名:曲霉菌属
拉丁学名:Aspergillus
分类学地位:真菌界Fungi;子囊菌门Ascomycota;
散囊菌纲Eurotiomycetes;散囊菌目Eurotiales;
曲菌科Aspergillaceae;曲霉属Aspergillus
曲霉菌属(Aspergillus)又称麹菌属、曲霉属,是一个由几百种多细胞霉菌菌种所组成的真菌菌属,其菌丝分支分隔,且分生孢子梗长在足细胞上不分枝,在许多气候与环境条件下皆可发现它们的踪影。[1]曲霉菌菌种繁多,除了是发酵工业的重要菌种,也是重要的食品变质菌类,或是可直接感染人类与动物,或在寄生饲料、粮食中产生毒素,曲霉属菌种目前至少有以下530种以上,如酸腐曲霉、针孢曲霉、白曲霉等。
1.1生物学特性
1.1.1培养特征
该属的成员皆具有能够在高渗透压环境中生长的能力,且该属的物种都非常好氧[2],常常能在氧气充足的环境下找到他们,并观察到他们呈现菌丝型态。
1.1.2形态学特征
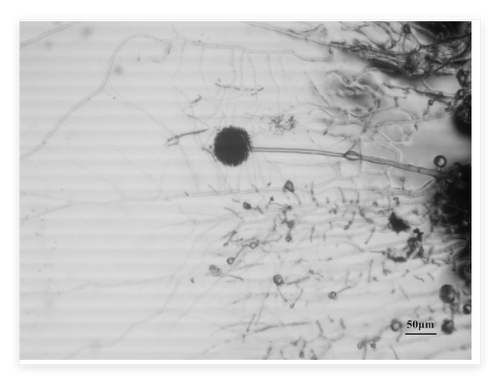 曲霉属包含的种类比较多,主要有黄曲霉、寄生曲霉、杂色曲霉、构巢曲霉等等,是一类可以产生生物毒素的菌属,曲霉的孢子颜色各异,是区分曲霉种类的主要依据[3]。黑曲霉菌丝有隔膜,为多细胞霉菌。菌丝体产生大量的分生孢子梗,分生孢子梗顶端膨大成为顶囊,一般呈球形。顶囊表面长满一层或两层辐射状小梗(初生小梗与次生小梗)。最上层小梗瓶状,顶端着生成串的球形分生孢子。孢子呈黑色。分生孢子梗生于足细胞上,并通过足细胞与营养菌丝相连。培养一周后,可看到明显的孢子脱落。连续观察2周,仍然可以观察到黑曲霉的产孢结构,分生孢子易观察。
曲霉属包含的种类比较多,主要有黄曲霉、寄生曲霉、杂色曲霉、构巢曲霉等等,是一类可以产生生物毒素的菌属,曲霉的孢子颜色各异,是区分曲霉种类的主要依据[3]。黑曲霉菌丝有隔膜,为多细胞霉菌。菌丝体产生大量的分生孢子梗,分生孢子梗顶端膨大成为顶囊,一般呈球形。顶囊表面长满一层或两层辐射状小梗(初生小梗与次生小梗)。最上层小梗瓶状,顶端着生成串的球形分生孢子。孢子呈黑色。分生孢子梗生于足细胞上,并通过足细胞与营养菌丝相连。培养一周后,可看到明显的孢子脱落。连续观察2周,仍然可以观察到黑曲霉的产孢结构,分生孢子易观察。
图1 黑曲霉显微镜图
黄曲霉:菌落表面初为淡黄绿色。在光学显微镜下观察,可以明显观察的菌丝细胞上形成分生孢子梗,辐射状,无色,顶端膨大形成顶囊,呈球形或半球形,分生孢子在小梗上链状着生长,其周围有小突起,呈球形。
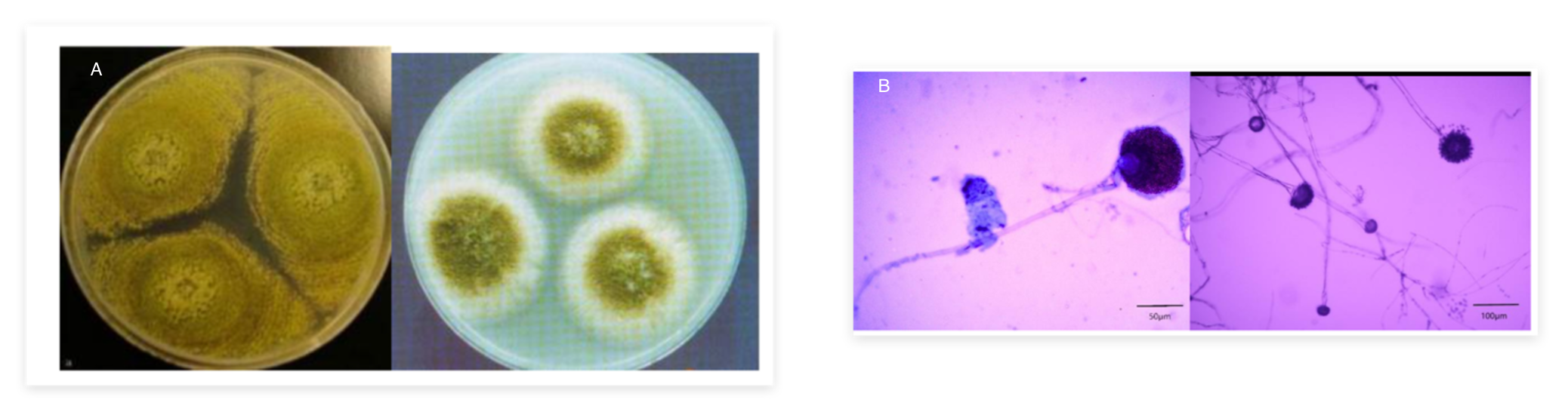
图2. 黄曲霉菌落和显微镜图。
A:菌落图;B:显微镜图
以及[4]如泡盛曲霉、贪黑曲霉等23种曲霉的形态学信息,展示部分如下。
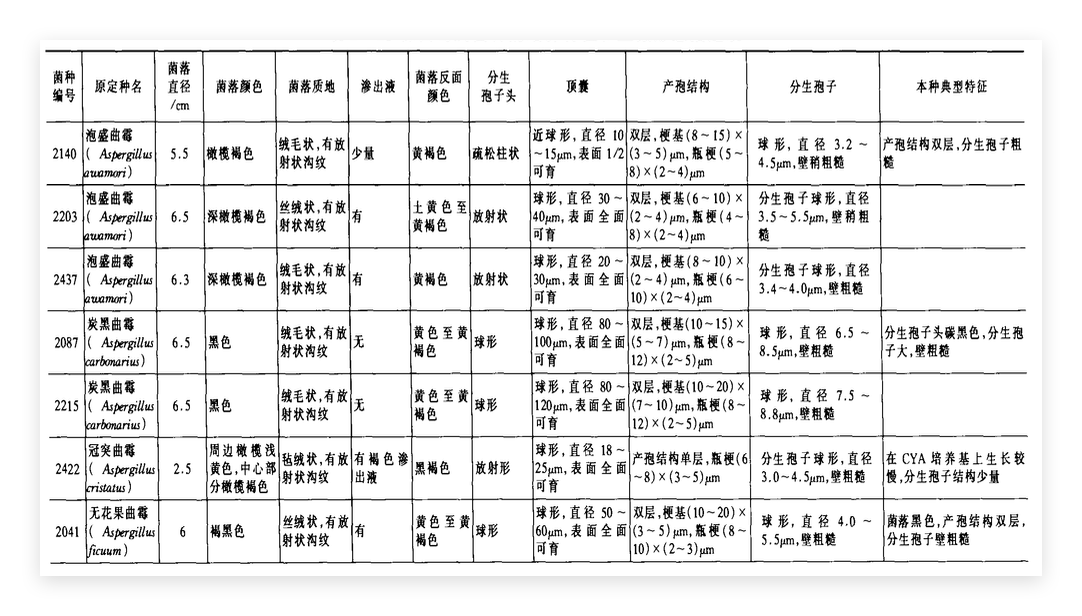
图3.23种曲霉形态学鉴定的部分展示
1.1.3生化特征
塔宾曲霉[5]:水解淀粉、明胶、过氧化氢、柠檬酸钠,不分解油脂、尿素.糖酵解试验产酸、产气.产硫化氢、不产氨.可利用蔗糖、麦芽糖和纤维二糖。
烟曲霉[6]具有在各种环境条件下生长的卓越能力。这包括具有挑战性的热条件(12-65°C)、酸性条件(pH 2.2-8.8)和营养条件(多种底物被多种糖基水解酶和蛋白酶降解)。
1.1.4分子生物学特征
黑曲霉:Andersen等[7]对黑曲霉的产酸株ATCC1015和产酶株CBS513.88进行相同培养条件下的转录组学比较分析,结果表明产酶菌株CBS513.88的参与糖酵解途径,TCA循环和氨基酸代谢有关的基因表达上调,尤其与苏氨酸、丝氨酸和色氨酸这3个氨基酸合成途径相关的基因上调显著,而这些氨基酸在葡萄糖淀粉酶(又名糖化酶,Glucoamylase,GlaA),tRNA合成酶,蛋白质转运子中含量较高;ATCC1015中参与生物氧化和电子传递链、碳水化合物和有机酸转运的基因显著上调。代谢流分析结果表明CBS513.88中3种氨基酸生物合成途径的通量至少是ATCC1015的2倍,与转录组的结果吻合。
黄曲霉:一些菌种,[8]包括A. flavus、A. pseudotamarii和A. togoensis,只产生B型黄曲霉毒素,而其他菌种,包括A. parasiticus、A. minisclerotigenes、A. mottae、A. nomius、A. novoparasiticus、A. arachidicola和A. korhogoensis,则既产生B型黄曲霉毒素,又产生G型黄曲霉毒素16、23。一些菌种还可能产生其他有毒的次生代谢产物,如环匹阿尼酸(CPA)。
曲霉属被定序的基因体大小分布大约从烟曲霉的29.3 Mb到米曲霉的37.1 Mb,然而本来被预估有9926 Mb,而米曲霉本来被预估有12071 Mb。至于产酶菌株黑曲霉的基因体大小为33.9 Mb,介于两者之间。
1.2分布、传播与致病性
1.2.1分布与传播
该属的成员皆具有能够在高渗透压环境中生长的能力,且该属的物种都非常好氧,常常能在氧气充足的环境下找到他们,并观察到他们呈现菌丝型态。正常来说,其菌体喜欢生长在碳源丰富的基质,像单糖或多糖丰富的地方。曲霉属常常为淀粉类食物(面包、米、马铃薯等)的污染源,也生长于许多植物及树种上。除了生长于营养丰富的基质上以外,曲霉属中的许多物种皆可在营养缺乏或缺少关键养分的环境中进行寡营养生长。黑曲霉是最好的例子,往往可以在潮湿的墙壁上发现它的踪影,为造成白粉病的主要菌种。
1.2.2致病性
有些曲霉属的物种造成人体及动物疾病。最常见的病原菌是烟曲霉和黄麹霉,他们制造黄曲毒素(是毒素亦是致癌物,并可污染如坚果类的食物)。最常见造成过敏反应的物种是烟曲霉和棒曲霉。还有些变种能制造霉菌毒素,其中包含黄曲毒素。还有一些会导致新生儿疾病。[9]烟曲霉(最常见的物种)造成的感染主要是肺部的感染,并且有可能由肺吲发炎造成快速的细胞坏死,也有传播的可能性。这物种可和其他霉菌感染区别,基于它无论在环境还是宿主都是以菌丝态存在。(不像白色念珠菌为二型性,在环境为菌丝态而在宿主为酵母态)。
1.3检测方法
1.鉴定烟曲霉(专利号:CN104046681A):
(1)提取待测烟曲霉菌株的总DNA;
(2)选取RPB2基因作为分子标记,即目的片段,设计特异性引物3条,分别为:
1)引物名称F2255,引物序列CCAACAAGCGTGTTCGTTCAG;
2)引物名称R3044,引物序列TGTCCGTGACGAGAGGCAAAT;
3)引物名称R3438,引物序列CTGCCGGGTCAGAATCTGT;
(3)待测烟曲霉菌株目的片段PCR扩增;
(4)琼脂糖凝胶电泳检测,根据电泳检测结果判断待测菌株是否为烟曲霉菌。
2.黄曲霉[10]
TLC法是检测黄曲霉素最为经典的方法,也是以前最为常用的方法,至今仍为一些检测机构所用,也是一种国标方法。其原理是针对不同的试样,用适宜的萃取溶剂将黄曲霉素从试样中萃取出来,经柱层析净化后,再在薄板上展开后分离。利用黄曲霉素的荧光特性,根据荧光斑点的强弱与标准比较确定其含量,对于一些组分很复杂的试样要双向展开,才能获得较高的灵敏度。
HPLC法是近年来发展起来的一种检测方法。其原理是在高效液相色谱仪上添加柱后衍生系统分离,再用荧光检测器测定。与其配套的柱后衍生系统有碘衍生化法、溴衍生化法及较为先进的电化学衍生化法和光化学衍生化法。当前,该方法大多用免疫亲和柱来净化、分离,其净化效果优异。该法能准确地分离不同种类的黄曲霉素(例如:AFB1、AFB2、AFG1和AFM1等),检测速度快且定性与定量准确,检测限低,可作为仲裁法使用。
1.4典型案例
1960年英国伦敦郊区爆发了“火鸡X病”(当时不清楚病因,故以此命名),因黄曲霉毒素而引起的约10万头火鸡急性中毒死亡,并在第2年证实其有强烈致癌性。解剖结果显示,所有死去的火鸡肝脏均出现了坏死现象,所有死去的火鸡都共同食用了一种饲料成分——花生粕,这种花生粕是榨油后的残渣,富含蛋白质,常被用作动物饲料。随后,科学家们对花生粕进行了深入的研究,揭露了其中的罪魁祸首——黄曲霉。这种真菌在感染花生粕后,会生成一种高度剧毒的物质,即黄曲霉素。值得注意的是,黄曲霉素的毒性极强,某些种类的毒性甚至超过了著名的毒药氰化钾。更令人担忧的是,黄曲霉素还是目前已知的最强致癌物之一。
1.5防治对策
避免潮湿环境,曲霉菌广泛存在于潮湿的环境中,如地下室、储物间、堆肥等。因此,避免长时间停留在这些环境中是预防曲霉病的重要措施。保持环境干燥、通风良好,有助于减少曲霉菌的滋生。
个人卫生习惯,勤洗手,尤其是在接触土壤、腐烂植物或有机物后,有助于减少曲霉菌的接触。此外,保持良好的个人卫生习惯,如避免与他人共用衣物、毛巾等,也有助于预防曲霉菌感染。
避免接触高风险环境,避免直接接触可能含有曲霉菌的环境,如腐烂的树叶、堆肥等。对于免疫功能低下的人群,应尽量避免进入高风险环境。
1.6危害等级与标准限值
(1)WHO/FAO标准。国际卫生组织(WHO)/世界粮农组织所属的食品法典委员会(CAC)推荐食品、饲料中黄曲霉毒素最大允许量标准为总量(B1+B2+G1+G2)小于15 μg/kg;牛奶中M1的最大允许量为0.5 μg/kg。
(2)南非标准。1990颁布了黄曲霉毒素的最大允许标准:食品中黄曲霉毒素总量小于10 μg/kg,其中黄曲霉毒素B1小于5 μg/kg。
(3)其他标准。印度标准是花生中黄曲霉毒素B1小于30 μg/kg;越南和阿根廷的标准为黄曲霉毒素B1小于20 μg/kg。
测定黄曲霉毒素测定的方法有薄层色谱法、高效液相色谱法、酶联免疫吸附测定法、质谱法、放射免疫测定法。这些方法中,国标方法“免疫亲和柱法”是现在[11]国际公认的比较经济有效的分析方法。有着较好的权威性和通用性,且为国外多个组织认可,被列为标准方法,如:美国公职分析化学家协会(AOAC);美国农业部联邦谷物检测中心(FGIS);美国食品药品行政署(US-FDA);中国出入境检验检疫局(CIQ)
黄曲霉毒素检测—“免疫亲和柱法”方法具体步骤如下:
1、试剂配制
(1)样品提取溶剂:甲醇/水(4/1,v/v)
(2)5 mmol磷酸盐缓冲溶液(PBS)(pH 7.2)母液配制:
1)称取50.14 g Na2HPO4·12H2O溶解于700 mL水中。
2)称取9.66 g NaH2PO4·H2O溶解于350 mL水中。
3)将上述两种溶液进行混合并加入42.5 g NaCl,配制成pH 7.2 5 mmol
磷酸盐缓冲溶液
(3)1 mmol磷酸盐缓冲溶液(PBS)(pH 7.2)工作液配制:
取200 mL的5 mmol磷酸盐缓冲溶液(pH 7.2)稀释于800 mL水中。
(4)磷酸盐缓冲溶液(PBS)/吐温(Tween)配制:取8 mL吐温-20稀释于92 mL pH 7.2磷酸盐缓冲溶液中。
(5)HPLC流动相配制:水/甲醇/乙腈(60/30/15,v/v)。
参考文献
[1] 刘警鞠, 张雨森, 陈娟 等. 曲霉属的现代分类命名研究进展. 生物技术通报, 2022, 38: 109-118.
[2] Silva R, Araripe JR, Rond inelli E.Gene expression in Chromobacteriumviolaceum.GenetMol Res, 2004, 3: 64-75.
[3] 沈萍, 陈向东《微生物学实验》4版. 高等教育出版社. 2007, 69-76.
[4] 姚粟, 李辉, 程池. 23株曲霉属菌种的形态学复核鉴定研究. 食品与发酵工业, 2006, 32: 37-43.
[5] 吴沣, 郝瑞霞, 鲁安怀 等. 塔宾曲霉的生物学特征及其对环境中Pb2+的固定作用研究. 环境科学学报, 2015, 35: 144-151.
[6] Abad A, Fernández-Molina J V, Bikandi J et al. What makes Aspergillus fumigatus a successful pathogen? Genes and molecules involved in invasive aspergillosis . Rev Iberoam Micol. 2010, 27: 155-182.
[7] 隋雨菲, 欧阳立明, 鲁洪中 等. 黑曲霉组学研究进展. 生物工程学报, 2016, 32: 1010-1025.
[8] Makhlouf, J., Carvajal-Campos, A., Querin et al.molecular and metabolic characterization of Aspergillus section Flavi in spices marketed in Lebanon. Scientific reports, 2019, 9, 5263.
[9] Cloherty J. Manual of neonatal care. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2012.
[10] 刘英, 胡建华, 刘春朝. 黄曲霉素毒理效应及检测方法. 生物加工过程, 2013, 11: 83-88.
[11] 刘先德. 黄曲霉毒素及其检测方法整体解决方案. 食品安全导刊, 2015: 95.
.png)
