1.福氏耐格里阿米巴(Naegleria fowleri)
物种名:福氏耐格里阿米巴
拉丁学名:Naegleria fowleri
分类学地位: 原生生物界Protista;变形虫门Amoebozoa;
变形虫纲Tublinomorpha;耐格里目Vahlkampfiida;
耐格里科Vahlkampfiidae;耐格里属Naegleria
福氏耐格里阿米巴(Naegleria fowleri)是一种自由生活的变形虫,属于耐格里属(Naegleria)。福氏耐格里阿米巴细胞为单核、无鞭毛的细胞,细胞质呈颗粒状。其大小约为8至15微米,细胞膜薄且柔软。福氏耐格里阿米巴能够在高温环境下生存,并在水中以阿米巴形态存在。其在特定条件下,能够通过鼻腔进入人体,尤其是在潜水、游泳等活动中发生感染。福氏耐格里阿米巴感染引发的主要疾病是致命的原发性阿米巴脑膜脑炎(PAM),该病症是一种急性、致命的脑部感染,通常表现为高烧、头痛、恶心、呕吐和神经系统症状[1]。
1.1生物学特性
1.1.1培养特征
福氏耐格里阿米巴可在无营养琼脂平板上培养,表面覆盖大肠埃希氏菌(E. coli)。在37℃下培养,阿米巴虫体会沿着细菌生长轨迹移动,形成透明带,表明其已摄取细菌。此外,也可在液体无菌培养基中培养。通过这些方法可以观察其不同的生活阶段[2-3]。
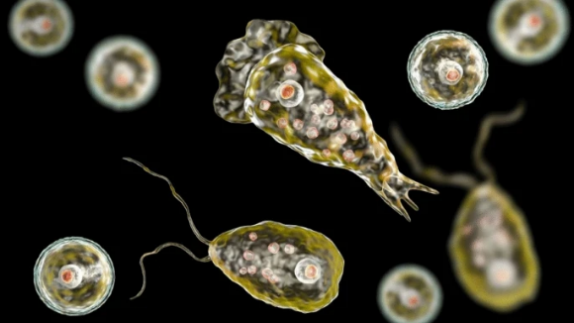
图1 福氏耐格里阿米巴
1.1.2形态学特征
福氏耐格里阿米巴是一种单细胞变形虫,具有三种主要的形态学特征:营养体、鞭毛体和囊体,每种形态在其生命周期中扮演不同的角色[4]。
营养体(Trophozoite):这是福氏耐格里阿米巴的活跃阶段,也是其引发感染的形态。营养体呈不规则的变形虫形态,细胞质通常是颗粒状,且核仁较大。它们通过伪足运动,在宿主的脑脊液中游走并吞噬细胞。这一阶段的大小可达40 µm以上,适应性强,能够在不同的环境中存活。营养体的形态变化使其具有强烈的趋化性和趋光性,能根据环境的变化不断调整自己的形态。
鞭毛体(Flagellate):在环境不利或低渗透溶液条件下,营养体可转变为鞭毛体。此时,Naegleria fowleri失去伪足,转变为具有两个鞭毛的形态,呈梨形或椭圆形。鞭毛体通常具有较强的运动能力,并能够在水中以鞭毛推动的方式移动,尽管这种形态在感染过程中较少见,但它在环境适应中具有重要作用。
囊体(Cyst):当外部环境极度不利时,福氏耐格里阿米巴的营养体会转化为囊体。这种形态通常具有圆形的外观,大小为7-15 µm,细胞壁厚且光滑。囊体能够在极端条件下存活,如低温或缺乏水分,它能在环境中长时间保持活性,直到条件恢复正常。囊体形态是福氏耐格里阿米巴生存的一种防御机制,能帮助其在不利环境中度过不适宜的生存期。
这三种形态在福氏耐格里阿米巴的生命周期中各有不同的功能,特别是在宿主感染过程中,营养体的变形和伪足运动是其致病性的重要特征。
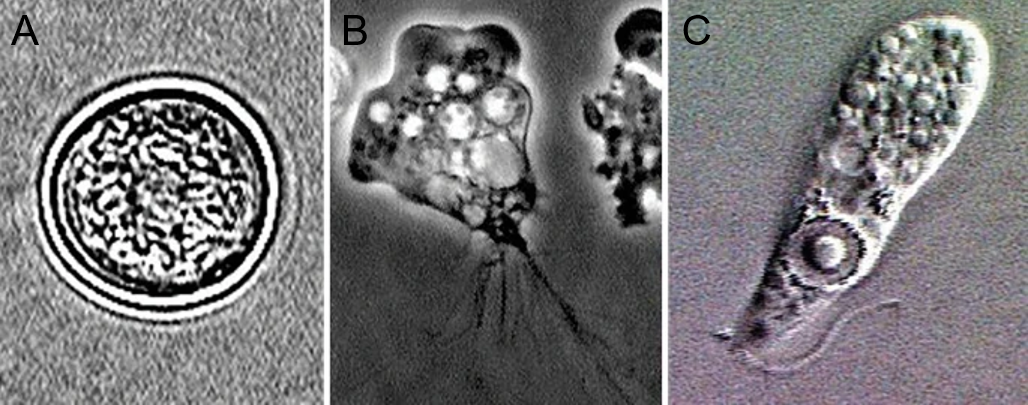
图2 福氏耐恪里阿米巴的不同形态
A:营养体,B:鞭毛体,C:囊体
1.1.3生化特征
福氏耐格里阿米巴是一种兼性厌氧的自由生活变形虫,能够在氧气丰富或缺乏的环境中生存。其主要通过吞噬细菌、藻类等微生物获取营养,并具有蛋白酶、脂肪酶和糖苷酶等酶活性,有助于摄取和分解宿主细胞。福氏耐格里阿米巴在环境恶劣时会转化为囊体,通过厚壁保护自己存活[5]。它对某些抗生素如磺胺类药物和青霉素表现出抗药性,这使得治疗原发性阿米巴脑膜脑炎(PAM)较为困难。其细胞壁在不同形态之间变化,营养体具有较薄的细胞壁,便于运动,而囊体则具有厚壁,增强了其在不利环境中的生存能力。福氏耐格里阿米巴的生化特征使其在不同环境中适应并具备致病性[3]。
1.1.4分子生物学特征
福氏耐格里阿米巴的分子生物学特征包括其基因组、蛋白质表达和分子机制的相互作用。其基因组为单倍体,大小约为2.2 Gb,包含大约12000个基因,这些基因与其致病性密切相关。基因组分析揭示了多个关键基因,参与不同生活史阶段的转变。福氏耐格里阿米巴利用表面抗原蛋白(SAG1和SAG3)与宿主细胞膜的糖类分子结合,帮助其突破宿主的免疫防线,促进侵染过程[3]。此外,福氏耐格里阿米巴的基因组中还包含编码肌动蛋白及相关运动蛋白的基因,这些基因促进伪足的运动,使其能够在宿主组织内迁移[6]。福氏耐格里阿米巴的免疫逃逸机制也与基因组中的免疫调节基因相关,这些基因能够通过调节免疫反应抑制如TNF-α和IL-6等免疫因子的释放,逃避宿主免疫系统的监视[7]。此外,福氏耐格里阿米巴还具备将营养体转化为鞭毛体的能力,这一过程与其基因组中的鞭毛相关基因密切相关,帮助其在不利的环境条件下适应和生存[8]。这些分子生物学特征使福氏耐格里阿米巴在环境中具有较强的生存能力,并能引发严重的致病反应。
1.2分布、传播与致病性
1.2.1分布与传播
福氏耐格里阿米巴是一种自由生活的变形虫,广泛分布于全球温暖的淡水环境中,如湖泊、河流、热泉以及工业或电厂的温水排放口。它也可能存在于土壤、热水器、管道和维护不当的游泳池中。全球已有381例PAM病例被记录,其中美国报告了164例,主要集中在南部州份,如德克萨斯州和佛罗里达州。然而,近年来,随着气候变化导致水温升高,北部州份的感染风险也在增加。巴基斯坦在2008年至2015年间报告了98例死亡病例,成为全球感染率第二高的国家。此外,澳大利亚昆士兰州的查尔维尔和奥加泰拉也在2025年首次确认了水源中存在该变形虫[9]。
1.2.2致病性
福氏耐格里阿米巴是一种水生自由生活的变形虫,能够通过鼻腔进入人体并引发严重的脑部感染。该病原体通过水流进入人体时,通常通过鼻腔进入,并沿着嗅神经进入大脑。它侵入中枢神经系统后,会引发致命的原发性阿米巴脑膜脑炎(PAM),该疾病通常表现为头痛、恶心、呕吐、发热和昏迷等症状。感染进展迅速,通常在感染后1至2周内致死。福氏耐格里阿米巴的致病机制与其在水中的活动方式密切相关。当水温升高时,变形虫的生长速度加快,增加了与人类接触的风险。该病原体通过其变形虫形态入侵脑部,通过分泌酶类物质破坏神经组织,引起脑细胞的坏死和出血。感染后死亡率超过97%,且目前无有效治疗方法。感染通常发生在温暖的淡水中,尤其是在夏季高温季节,然而,口服水并不会引发感染,只有水进入鼻腔才会导致病变[5][9]。
1.3检测方法
福氏耐格里阿米巴的检测方法主要包括显微镜检查、分子生物学技术和培养法。显微镜检查是最常用的初步检测方法,通过从患者脑脊液或其他受感染组织中取样,使用低温显微镜进行直接观察,能够发现变形虫的形态特征。然而,显微镜检查对细胞数量较少或变形虫活性不高的样本可能不敏感,因此需要结合其他方法。分子生物学技术,如聚合酶链反应(PCR),已被广泛应用于福氏耐格里阿米巴的检测。PCR能够高灵敏度地检测出变形虫的DNA,尤其适用于脑脊液和其他体液样本的检测。此外,培养法也常用于确认感染,通常通过将样本接种到特定的培养基上,在适宜的温度下培养变形虫,并通过生长观察和形态学特征进一步确认感染。虽然培养法较为繁琐且时间较长,但它能够提供病原体的进一步信息,包括其耐药性和其他生物学特性[5][9]。
1.4典型案例
2025年8月,澳大利亚昆士兰州的查尔维尔(Charleville)和奥加泰拉(Augathella)首次在其自来水系统中检测到致命的“脑食变形虫”福氏耐格里阿米巴。该变形虫通常存在于温暖的淡水环境中,若受污染的水进入鼻腔,可能引发致命的原发性阿米巴脑膜脑炎(PAM)。尽管饮用水被认为是安全的,但当地卫生部门提醒居民在洗澡、洗脸或其他活动中避免水进入鼻腔。这一发现引发了对热水系统和自来水管道卫生状况的关注,尤其是在大温泉盆地(Great Artesian Basin)等未加氯的水源地区。昆士兰州自2000年以来已有6人死于福氏耐格里阿米巴感染,均与私人水源系统有关[10][11]。
1.5防治对策
福氏耐格里阿米巴的防治对策主要集中在水源管理和公共卫生预防措施上。首先,针对可能存在该变形虫的水源,建议定期进行水质监测,特别是在温暖的水域和未经过滤的私人水源中,确保水中不存在致病性变形虫。其次,为了减少人群感染风险,公共卫生部门应加强对居民的健康教育,提醒公众避免在温暖的淡水中进行潜水、游泳等活动,尤其是在高温季节。同时,应鼓励居民在使用水源进行鼻腔冲洗或其他类似活动时,使用经过处理或煮沸的水。对于游泳池,应严格执行水质管理标准,包括使用适当的氯化处理,以减少变形虫的生长。此外,对于废水处理厂和工业排放的水,必须采取有效的过滤和消毒措施,以减少水源的污染。通过这些综合性措施,可以有效降低福氏耐格里阿米巴的传播风险,保护公众健康[6][9]。
参考文献
- Siddiqui R, Ali IKM, Cope JR et al. Biology and pathogenesis of Naegleria fowleri. Acta tropica, 2016, 164: 375-394.
- Borkens Y. The Pathology of the Brain Eating Amoeba Naegleria fowleri. Indian J Microbiol, 2024, 64: 1-11.
- Schuster FL. Cultivation of pathogenic and opportunistic free-living amebas. Clin Microbiol Rev, 2002, 15: 342-354.
- https://en.wikipedia.org/wiki/Primary_amoebic_meningoencephalitis?utm_source=chatgpt.com
- https://www.cdc.gov/naegleria/about/index.html
- Kofman A, Guarner J. Infections Caused by Free-Living Amoebae. J Clin Microbiol, 2022, 60: e0022821.
- Francine MC, Guy A. Cabral, The immune response to Naegleria fowleri amebae and pathogenesis of infection. FEMS immunology and medical microbiology, 2007, 51: 243-259.
- Liechti N, Schürch N, Bruggmann R, Wittwer M. The genome of Naegleria lovaniensis, the basis for a comparative approach to unravel pathogenicity factors of the human pathogenic amoeba N. fowleri. BMC Genomics, 2018, 19: 1-11.
- Gharpure R, Bliton J, Goodman A, Ali IKM, Yoder J, Cope JR. Epidemiology and Clinical Characteristics of Primary Amebic Meningoencephalitis Caused by Naegleria fowleri: A Global Review. Clin Infect Dis, 2021, 73: e19-e27.
- https://www.abc.net.au/news/2025-08-11/naegleria-fowleri-murweh-shire-rural-queensland-drinking-water/105636078
- https://britbrief.co.uk/environment/water/brain-eating-amoeba-found-in-queensland-water-supply.html
.png)
