1.巨细胞病毒(Cytomegalovirus)
物种名:巨细胞病毒
拉丁学名:Cytomegalovirus
分类学地位:香港病毒界Heunggongvirae;衣壳病毒门Peploviricota;
疱疹病毒纲Herviviricetes;疱疹病毒目Herpesvirales;
疱疹病毒科Herpesviridae;巨细胞病毒属Cytomegalovirus
巨细胞病毒(CMV)属于疱疹病毒科β疱疹病毒亚科,是一种广泛存在于自然界且具种属特异性的双股DNA病毒。人类感染的主要病原体为人巨细胞病毒(HCMV,又称人疱疹病毒5型)。该病毒最早于1881年被发现,因能使感染细胞显著增大并形成典型包涵体而得名。CMV主要在唾液腺中感染,可通过唾液、生殖道分泌物、胎盘、输血或器官移植等途径传播。多数人在幼儿期即发生初次感染,常为隐性或潜伏状态,但对新生儿、HIV感染者及器官移植患者等免疫缺陷人群可引起严重甚至致命的全身感染。
1.1生物学特性
1.1.1培养特征
巨细胞病毒在体外培养中具有明显的特征,其最显著的一点是严格的种属特异性,只能感染人类细胞,主要在人胚肺成纤维细胞(如MRC-5细胞系)中有效增殖,而无法在其他动物细胞中生长[1]。常用的培养条件为含10%小牛血清的1640或DMEM培养基,在37℃、5% CO₂孵箱中维持单层细胞生长[2,3]。HCMV的增殖速度较慢,初次分离时往往需要30-40天才能观察到明显的细胞病变效应(CPE),传统培养方式通常需5–30天才能出具结果,因此费时费力。除成纤维细胞外,部分临床分离株(如TB40/E)在上皮细胞、内皮细胞及平滑肌细胞中也可复制,但效率依毒株差异而异,实验室长期传代的株(如AD169)则表现为成纤维细胞适应性强而组织嗜性减弱[1]。为了缩短检测周期,现代实验室常用离心辅助的壳瓶培养法,将样本接种后离心促进病毒进入细胞,16–48小时内即可通过免疫荧光检测早期抗原(如IE/pp72)快速判定阳性;同时,pp65抗原血症法和PCR等核酸检测已成为临床早期诊断的重要补充,尤其在新生儿先天性CMV感染和移植人群监测中应用广泛[4]。需要注意的是,培养阳性结果仅能提示存在病毒排出,并不能单独作为活动性感染的判定依据,必须结合患者免疫状态和临床表现综合分析。
1.1.2形态学特征
巨细胞病毒是一种典型的包膜DNA病毒,其形态学结构与单纯疱疹病毒(HSV)极为相似,整体呈球形至多形性,具有二十面体对称性(T=16),病毒粒子直径约150-200 nm。其超微结构为“三层构造”(图1A):外层为带有多种糖蛋白的脂质包膜,中层为富含蛋白的基质层(tegument),内层为近似二十面体的对称衣壳,内部封装不分段的线性双链DNA(图1B)。感染细胞后,约3-4天可在细胞核内见到核衣壳装配,并通过核膜芽生转运至胞浆囊泡中,最终形成完整的病毒颗粒;此过程中,核内可见大量衣壳与网状物紧密结合[5–7]。HCMV可感染多种人类细胞,尤其是血管内皮细胞和白细胞,并在内皮细胞中形成典型的包涵体。其最具特征性的病理学表现为感染细胞显著肿大变圆,细胞核增大,并形成周围带有“晕轮”的大型嗜酸性核内包涵体(图1D),即特征性的“猫头鹰眼”样病变,同时可见核周和细胞质包涵体及细胞排列紊乱,导致细胞膨胀和特殊形态改变,这是“巨细胞病毒”名称的来源[8]。这些独特的形态学特征不仅揭示了病毒的结构与复制特点,也是组织学诊断CMV感染的重要依据,但临床确诊仍需结合抗原或核酸检测等实验室方法。
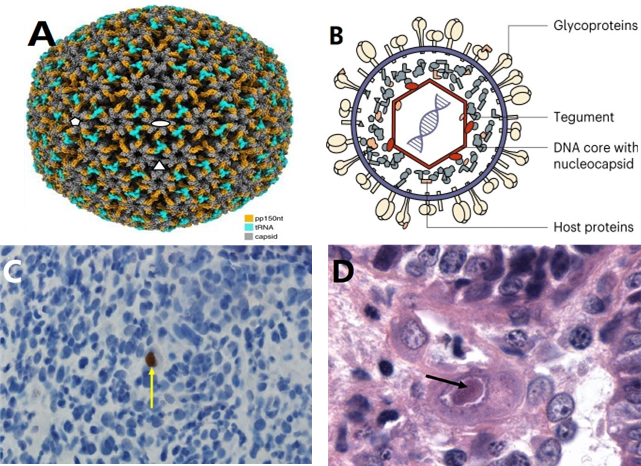
图1 巨细胞病毒结构特征
A:HCMV病毒粒子的二十面体重建[6],B:HCMV病毒粒子层的示意图[7]
C:CMV免疫染色,放大倍数×400[9],D:CMV结肠炎患者的活检标本显示了典型的“猫头鹰眼”核内包涵体(箭头)和胞浆内包涵体[4]
1.1.3生化特征
巨细胞病毒二十面体对称的蛋白衣壳主要由主要衣壳蛋白(MCP, pUL86)构成,形成稳定的结构核心;基质层中含有多种关键蛋白,如pp65(pUL83)、pp71(pUL82)和pp150,这些蛋白在病毒感染初期即被释放,参与免疫调节与病毒复制启动,其中pp65是临床免疫检测中的重要抗原成分;包膜表面镶嵌多种糖蛋白复合物(图2),包括gB(UL55)、gH/gL(UL75/UL115)、gM/gN以及五聚体复合物(gH/gL/UL128-131),这些糖蛋白介导病毒与宿主细胞的结合与融合,决定其细胞嗜性,并作为中和抗体的主要靶标[10–13]。HCMV具有稳定的物理化学特性,通常呈冻干粉末形态,无腐蚀性、不易燃、不吸湿、无刺激性,适合在特定条件下长期保存。在酶学特征方面,病毒编码DNA依赖的DNA聚合酶(UL54)和蛋白激酶UL97,前者是膦甲酸钠等抗病毒药物的作用靶点,后者可磷酸化更昔洛韦并作为马拉韦罗的靶标,两类酶均与抗病毒治疗的疗效和耐药密切相关[14,15]。临床上,基于病毒蛋白和核酸的生化检测方法广泛用于活动性感染的诊断,如pp65抗原血症检测可识别外周血白细胞中的病毒蛋白,而病毒DNA的定量PCR虽属分子检测范畴,但其基础仍依赖于病毒颗粒中稳定存在的DNA分子,反映病毒载量。这些结构与蛋白特征共同构成了CMV在生化层面的核心属性。
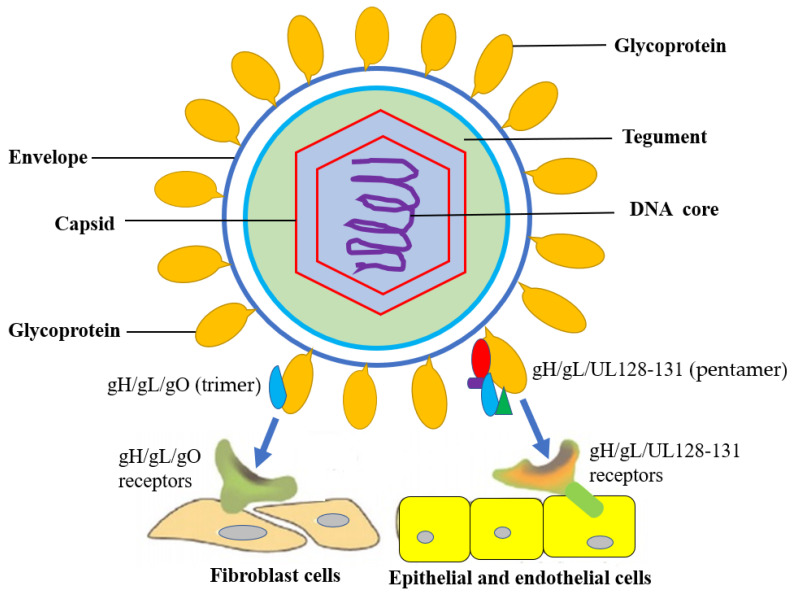
图2 巨细胞病毒结构特征HCMV结构和进入宿主细胞[13]。
1.1.4分子生物学特征
人巨细胞病毒是β疱疹病毒亚科的重要成员,其基因组约235-250 kb,是人类疱疹病毒中最大的之一,具有典型E型结构,由长区(UL)与短区(US)两段独特区组成,并被成对的重复序列(TRL/IRL、TRS/IRS)夹着,可形成四种基因组异构体,端部含有pac1/pac2包装信号和a序列[16–18]。实验室长期传代株(如AD169、Towne)常缺失ULb′区(含UL128–131、RL13等),导致组织嗜性减弱,而临床株则保持完整[19]。
在基因表达方面,HCMV展现出严格的三级转录时序(立即早期IE→早期E→晚期L)[20],其中MIE增强子–启动子(MIEP)是核心驱动元件,IE1和IE2蛋白是关键转录调控因子,能够调节染色质状态并在病毒与宿主基因表达中发挥核心作用[21]。病毒DNA复制发生在宿主细胞核内的复制区室,以OriLyt为起点进行滚环复制,生成串联体后经pac1/pac2信号切割并包装进入衣壳,随后通过核外排复合体(UL50/UL53等)出核,并在高尔基–内体网络中完成包膜与成熟[18]。
HCMV能够在髓系前体和单核细胞中建立潜伏感染,其机制以IE基因沉默和染色质抑制为核心,UL133–UL138多顺反子位点及病毒miRNA(如miR-UL112-1靶向IE1mRNA)在潜伏与再激活平衡中发挥重要作用[22,23](图3)。病毒的免疫逃逸机制十分复杂,包括US2/US3/US6/US11下调MHC-I抗原递呈通路,UL18作为MHC-I类似物结合LILRB1抑制NK细胞,UL40信号肽可稳定HLA-E以避免NK细胞杀伤;此外pp71、pp65等还能干扰先天免疫的PRR–干扰素信号通路[24–27]。遗传学研究表明,HCMV在宿主体内具有高度多态性,尤其是包膜糖蛋白和免疫调控基因簇(如RL11家族、UL1–UL11),表现出接近某些RNA病毒的变异度,这种遗传多样性与其广泛的宿主适应性及免疫逃逸能力密切相关[28]。
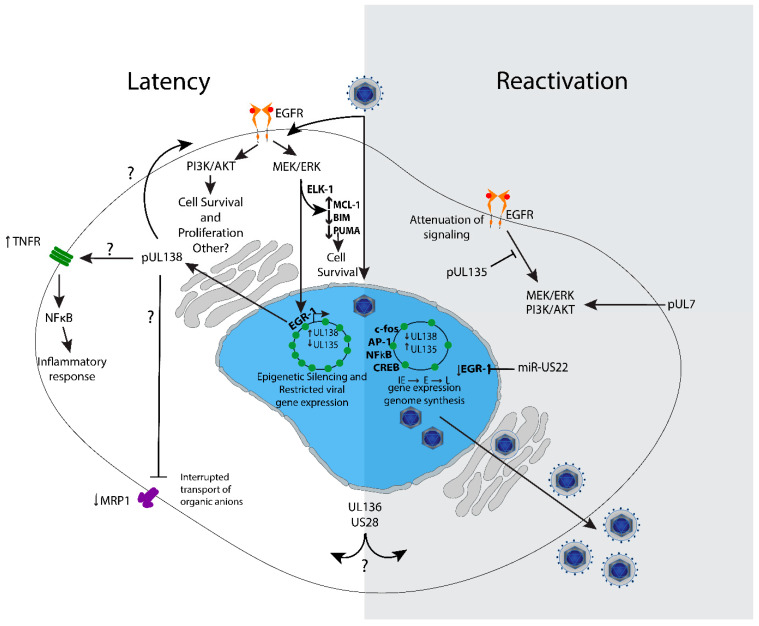
图3 UL133-UL138病毒-宿主相互作用和信号传导影响潜伏期和重新激活的模型[22]。
1.2分布、传播与致病性
1.2.1分布与传播
巨细胞病毒具有全球广泛分布,几乎无处不在,是人类最常见的病毒感染之一。系统综述与荟萃分析显示,全球一般人群CMV血清阳性率约83%,育龄妇女约86%,但不同地区、国家乃至同一国家内部存在显著差异:发达国家成人感染率约为45%-70%,而低中收入国家往往接近100%;在WHO区域比较中,东地中海地区最高,欧洲最低(约66%)[29,30]。这种差异与地理位置、社会经济水平、教育程度、人口密度和族群背景密切相关。先天性CMV(cCMV)是全球最常见的先天性感染,出生患病率约0.67%,且低中收入国家的负担是高收入国家的3倍[31]。传播方面,CMV主要依赖体液传播,包括唾液、尿液、血液、泪液、精液和母乳等,密切、持续的接触更易导致感染;性接触也是重要途径。母婴传播尤为关键,可通过胎盘(最主要、危害最大)、分娩时接触产道分泌物或哺乳期传染给新生儿。医源性传播也不可忽视,输血、器官移植或造血干细胞移植均可能将病毒传给易感者,特别是免疫功能低下人群。儿童在传播中扮演重要角色,尤其是托幼阶段的幼儿可长期排出病毒,使得与其密切接触的家长、看护或医护人员感染风险升高。总体来看,CMV的分布与传播受到社会经济水平、人口拥挤度、职业暴露及个体免疫状态的显著影响,呈现出明显的地区异质性和人群差异。
1.2.2致病性
巨细胞病毒的致病性主要体现在其广泛的组织嗜性、终生潜伏与再激活能力、复杂的免疫逃逸策略以及直接的细胞与组织损伤。病毒入侵依赖于两类关键糖蛋白复合物:三聚体gH/gL/gO介导其进入成纤维细胞,而五聚体gH/gL/UL128/UL130/UL131A则赋予其对上皮细胞、内皮细胞及部分髓系细胞的高度嗜性,从而奠定了其在宿主体内广泛传播与器官损害的基础[32–34]。与其他疱疹病毒类似,CMV能够在CD34⁺造血前体细胞及单核-髓系细胞中建立潜伏状态,当宿主免疫受损(如移植、化疗或HIV感染)时再激活,导致肺炎、肝炎、脑炎、结肠炎及视网膜炎等严重的器官性疾病,是免疫抑制人群重要的发病与死亡原因之一[35]。
在免疫学层面,CMV形成了系统性的免疫调控网络(图4A):如US2、US3、US6和US11蛋白通过下调MHC-I分子削弱抗原呈递,UL18作为MHC-I同源体与抑制性受体结合以阻断细胞毒性T细胞作用;UL40多肽通过调控HLA-E影响自然杀伤(NK)细胞活性;UL111A编码的病毒IL-10同源体(cmvIL-10)模拟宿主IL-10的功能,抑制树突状细胞活化和T细胞反应,在潜伏与裂解期均能维持免疫抑制并促进病毒持续存在(图4B)。这些机制协同作用,使CMV能够在宿主体内实现长期潜伏、周期性再激活及持续免疫干扰[25,36–39]。
在病理学层面,CMV感染导致细胞显著增大并形成典型的核内包涵体,表现为“猫头鹰眼”样改变,是病理诊断的重要特征。器官特异性损害方面,CMV视网膜炎常见于免疫缺陷患者,其病灶典型表现为大片白色坏死区伴随出血条纹,形成高度特征性的坏死性视网膜改变,若未及时控制可进展至严重视力丧失或失明[40]。
在先天性感染中,CMV是最常见的宫内感染病原体,是非遗传性感音神经性听力损失的首要病因,并可引起脑室周围钙化、神经发育障碍及长期神经感觉功能缺陷,提示其对中枢神经系统具有高度致病性[41]。除此之外,慢性CMV感染通过内皮细胞感染、免疫持续激活及促炎/促凝途径,被认为与移植并发症加重及动脉粥样硬化等慢性疾病进展相关[42]。
综上,CMV的致病性不仅源于直接的细胞病变,还包括其高度适应性的潜伏-再激活循环和复杂的免疫逃逸机制,与宿主免疫系统的长期博弈决定了其在新生儿缺陷、免疫抑制人群重症疾病及慢性病过程中的重要病理学与临床学意义。
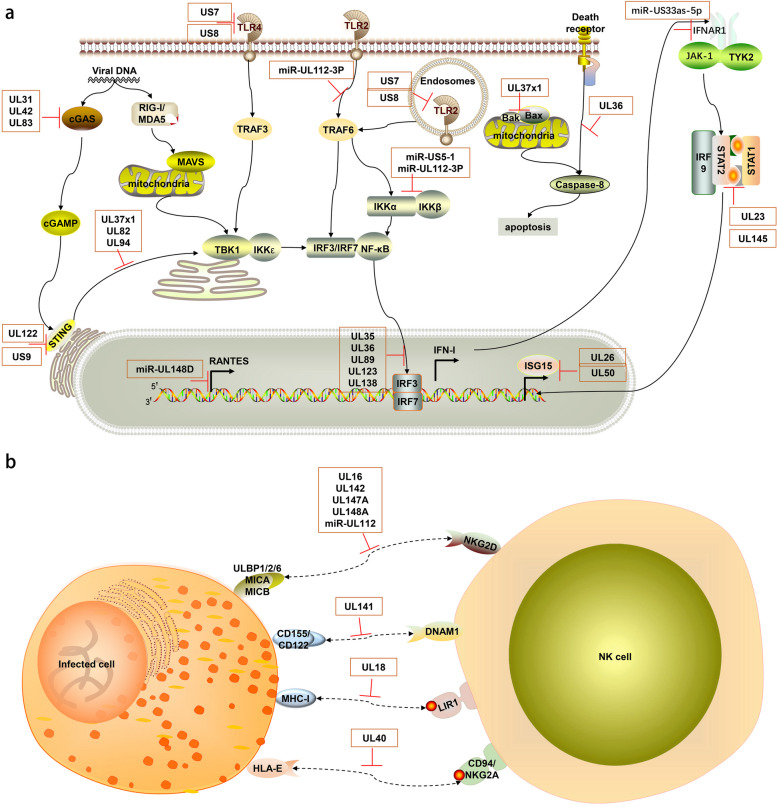
图4 HCMV逃避宿主先天免疫途径的机制示意图[42]。
A:人巨细胞病毒(HCMV)通过多种蛋白和miRNA抑制宿主的先天免疫反应
B:HCMV逃避NK细胞反应。
1.3检测方法
(1)实时荧光定量PCR(RT-qPCR)[43]:实时荧光定量PCR是目前临床检测巨细胞病毒(CMV)DNA的首选方法,被广泛用于血液、血浆、全血及体液样本的定量监测,也是国家和国际指南推荐的标准手段。其原理是提取临床样本中的核酸后,用针对CMV保守基因区(常见UL83、UL54、UL55等)的特异性引物与荧光探针进行扩增反应。在扩增过程中,TaqDNA聚合酶5’→3’外切酶活性裂解探针,释放荧光基团,从而实现荧光信号的实时累积检测。以UL83(pp65)区为例,常见的引物和探针为:
表1 巨细胞病毒RT-PCR引物序列
| 名称 | 序列 |
| 正向引物 | 5′-GTCAGCGTTCGTGTTTCCCA-3′ |
| 反向引物 | 5′-GGGACACAACACCGTAAAGC-3′ |
| 探针 | 5’FAM-CCCGCAACCCGCAACCCTTCATG-TAMRA-3′ |
典型反应体系可包括MgCl₂、dNTP(含dUTP)、引物/探针及AmpliTaq Gold等,循环条件如95°C 10 min→45个循环(95°C 15 s、65°C 1 min)。
该方法具有灵敏度高、可定量、标准化程度高的优势,能精确监测病毒负荷变化,是移植或免疫抑制人群随访与治疗决策的核心检测手段。但其局限在于:对不同靶基因/引物敏感性存在差异,需使用标准品(如WHO国际单位或国家参考物)建立标准曲线,保证实验室间结果可比性;同时对实验室设备和质量控制要求较高。
(2)pp65抗原检测[44]:pp65抗原检测是一种经典的非分子学方法,过去在临床上被广泛用于监测CMV感染,尤其在PCR尚未普及时被视为“金标准”。其原理是检测外周血白细胞中CMV主要基质蛋白pp65的表达:收集新鲜EDTA外周血,需在采样后6 h内处理,通过红细胞裂解或沉降法获得白细胞,制备玻片后进行固定与透化,再用抗CMVpp65单克隆抗体孵育,结合荧光或酶标二抗进行显色,最后在显微镜下计数核内或胞质内阳性细胞数,并以每2×10⁵白细胞中阳性细胞数作为结果。该方法的优点是能够直接反映病毒蛋白表达,即提示有病毒复制的活跃细胞,在一定程度上与临床疾病风险高度相关,且在设备要求较低的条件下仍可应用。
1.4典型案例
先天性CMV感染是最具代表性的病例类型之一。患儿常在出生时表现出小头畸形、脑室扩大、室周钙化、黄疸、肝脾肿大、出血点及神经系统异常等临床与影像学特征,实验室检查可见血小板减少和肝功能异常。产前超声可提示脑室扩大,出生后通过CT或颅脑超声进一步证实。该类病例凸显了先天性CMV的典型临床组合:多系统受累(神经系统+肝脾+血液),且在资源有限地区也能通过临床表现加以识别。文献报道中,一项大规模新生儿病例分析显示,多数患儿存在上述组合症状,典型影像学表现(如小头畸形和钙化)尤具诊断意义[45]。
另一类典型案例出现在原本健康的成人中,尽管罕见,却极具警示意义。文献报道一位免疫功能正常的女性患者,因原发CMV感染而出现严重的肺部损害和中枢神经系统受累,病程进展迅速,最终因多脏器功能衰竭而不幸死亡。另有报道指出,免疫健全成人可因CMV引发播散性血管内凝血(DIC),临床表现为凝血功能紊乱和多系统衰竭,虽然经抗病毒药物(如valganciclovir)治疗可获部分缓解,但病程依旧凶险。这类病例的典型意义在于提醒临床医生:即使在非免疫抑制人群中,CMV也可能导致严重甚至致命的并发症,不应仅将其视为免疫低下人群的“机会性感染”[46]。
1.5防治对策
巨细胞病毒防治策略主要针对高危人群,包括孕妇、移植患者及免疫受损者等。孕期防控强调一级预防,主要通过卫生教育(如勤洗手、避免与幼儿共用餐具等)显著降低母体感染及先天性CMV发生率;若孕妇已感染,则可尝试二级预防措施,包括高免疫球蛋白(HIG)或大剂量valaciclovir等,临床研究显示HIG在降低母婴传播及新生儿异常率方面优于valaciclovir[47],而疫苗仍处于实验阶段,保护效力有限。对于固体器官或造血干细胞移植受者,防治核心在于“普遍预防”与“前瞻性治疗”两大策略,前者通过术后常规使用ganciclovir或valganciclovir可显著减少CMV病发和死亡,但存在白细胞减少和晚发性CMV风险;后者则依赖血液学监测,发现病毒学阳性后立即启动治疗,能减少药物暴露和毒性[48]。总体而言,CMV防治以“预防为主、监测结合、抗病毒药物干预”为核心,不同人群和临床场景应采取个体化措施。
参考文献
[1] Wang D, Shenk T. Human cytomegalovirus UL131 open reading frame is required for epithelial cell tropism. Journal of Virology, 2005, 79: 10330-10338.
[2] Borst EM, Hahn G, Koszinowski UH, et al. Cloning of the Human Cytomegalovirus (HCMV) Genome as an Infectious Bacterial Artificial Chromosome in Escherichia coli : a New Approach for Construction of HCMV Mutants. Journal of Virology, 1999, 73: 8320-8329.
[3] 周亚滨, 张晓梅, 彭莹. HCMV-towne-GFP重组巨细胞病毒及其制备方法与应用: CN101319202A. 2008, 12: 10.
[4] Dioverti MV, Razonable RR. Cytomegalovirus. Microbiology Spectrum, 2016, 4: 4.4.20.
[5] Li Z, Pang J, Dong L, et al. Structural basis for genome packaging, retention, and ejection in human cytomegalovirus. Nature Communications, 2021, 12: 4538.
[6] Liu YT, Strugatsky D, Liu W, et al. Structure of human cytomegalovirus virion reveals host tRNA binding to capsid-associated tegument protein pp150. Nature Communications, 2021, 12: 5513.
[7] Bogdanow B, Gruska I, Mühlberg L, et al. Spatially resolved protein map of intact human cytomegalovirus virions. Nature Microbiology, 2023, 8: 1732-1747.
[8] Olyaee SAB, Sabahi F, Rostaie MH, et al. Growth and isolation of human cytomegalovirus on a new human fetal foreskin fibroblast-derived cell line in iran. Iranian Journal of Biotechnology, 2003, 1: 247.
[9] Inayat F, Hussain Q, Shafique K, et al. Cytomegalovirus colitis in immunocompetent patients. Cureus, 8: e869.
[10] Varnum SM, Streblow DN, Monroe ME, et al. Identification of proteins in human cytomegalovirus (HCMV) particles: The HCMV proteome. Journal of Virology, 2004, 78: 10960-10966.
[11] Reyda S, Tenzer S, Navarro P, et al. The tegument protein pp65 of human cytomegalovirus acts as an optional scaffold protein that optimizes protein uploading into viral particles. Journal of Virology, 2014, 88: 9633-9646.
[12] Tomtishen IIIJP. Human cytomegalovirus tegument proteins (pp65, pp71, pp150, pp28). Virology Journal, 2012, 9: 22.
[13] Chen SJ, Wang SC, Chen YC. Challenges, recent advances and perspectives in the treatment of human cytomegalovirus infections. Tropical Medicine and Infectious Disease, 2022, 7: 439.
[14] Bottino P, Pastrone L, Curtoni A, et al. Antiviral approach to cytomegalovirus infection: An overview of conventional and novel strategies. Microorganisms, 2023, 11: 2372.
[15] Prichard MN. Function of human cytomegalovirus UL97 kinase in viral infection and its inhibition by maribavir. Reviews in medical virology, 2009, 19: 215-229.
[16] Sijmons S, VanRanst M, Maes P. Genomic and functional characteristics of human cytomegalovirus revealed by next-generation sequencing. Viruses, 2014, 6: 1049-1072.
[17] VanDamme E, VanLoock M. Functional annotation of human cytomegalovirus gene products: An update. Frontiers in Microbiology, 2014, 5: 218.
[18] Sijmons S, Thys K, Mbong NM, et al. High-throughput analysis of human cytomegalovirus genome diversity highlights the widespread occurrence of gene-disrupting mutations and pervasive recombination. Journal of Virology, 2015, 89: 7673-7695.
[19] Collins-McMillen D, Buehler J, Peppenelli M, et al. Molecular determinants and the regulation of human cytomegalovirus latency and reactivation. Viruses, 2018, 10: 444.
[20] Kalejta RF. Tegument proteins of human cytomegalovirus. Microbiology and Molecular Biology Reviews : MMBR, 2008, 72: 249-265.
[21] Ball CB, Li M, Parida M, et al. Human cytomegalovirus IE2 both activates and represses initiation and modulates elongation in a context-dependent manner. mBio, 13: e00337-22.
[22] Mlera L, Moy M, Maness K, et al. The role of the human cytomegalovirus UL133-UL138 gene locus in latency and reactivation. Viruses, 2020, 12: 714.
[23] Lee SH, Caviness K, Albright ER, et al. Long and short isoforms of the human cytomegalovirus UL138 protein silence IE transcription and promote latency. Journal of Virology, 2016, 90: 9483-9494.
[24] Patel M, Vlahava VM, Forbes SK, et al. HCMV-encoded NK modulators: Lessons from in vitro and in vivo genetic variation. Frontiers in Immunology, 2018, 9: 2214.
[25] Prod’homme V, Tomasec P, Cunningham C, et al. Human cytomegalovirus UL40 signal peptide regulates cell surface expression of the natural killer cell ligands HLA-E and gpUL18. Journal of immunology (Baltimore, Md. : 1950), 2012, 188: 2794-2804.
[26] Forrest C, Gomes A, Reeves M, et al. NK cell memory to cytomegalovirus: Implications for vaccine development. Vaccines, 2020, 8: 394.
[27] Fu YZ, Su S, Gao YQ, et al. Human cytomegalovirus tegument protein UL82 inhibits STING-mediated signaling to evade antiviral immunity. Cell Host & Microbe, 2017, 21: 231-243.
[28] Renzette N, Bhattacharjee B, Jensen JD, et al. Extensive genome-wide variability of human cytomegalovirus in congenitally infected infants. PLoS pathogens, 2011, 7: e1001344.
[29] Zuhair M, Smit GSA, Wallis G, et al. Estimation of the worldwide seroprevalence of cytomegalovirus: A systematic review and meta-analysis. Reviews in Medical Virology, 2019, 29: e2034.
[30] AlMana H, Yassine HM, Younes NN, et al. The current status of cytomegalovirus (CMV) prevalence in the MENA region: A systematic review. Pathogens, 2019, 8: 213.
[31] Ssentongo P, Hehnly C, Birungi P, et al. Congenital cytomegalovirus infection burden and epidemiologic risk factors in countries with universal screening. JAMA Network Open, 2021, 4: e2120736.
[32] Ciferri C, Chandramouli S, Donnarumma D, et al. Structural and biochemical studies of HCMV gH/gL/gO and pentamer reveal mutually exclusive cell entry complexes. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112: 1767-1772.
[33] Paradowska E, Jabłońska A, Studzińska M, et al. Distribution of the CMV glycoprotein gH/gL/gO and gH/gL/pUL128/pUL130/pUL131A complex variants and associated clinical manifestations in infants infected congenitally or postnatally. Scientific Reports, 2019, 9: 16352.
[34] Ai Y, Wu C, Zhang M, et al. Neutralization epitopes in trimer and pentamer complexes recognized by potent cytomegalovirus-neutralizing human monoclonal antibodies. Microbiology Spectrum, 2022, 10: e0139322.
[35] L S, B W, S A, et al. Human Cytomegalovirus Latency and Reactivation in Allogeneic Hematopoietic Stem Cell Transplant Recipients. Frontiers in microbiology, 2019, 10.
[36] Prod’homme V, Griffin C, Aicheler RJ, et al. The human cytomegalovirus MHC class I homolog UL18 inhibits LIR-1+ but activates LIR-1- NK cells. Journal of Immunology (Baltimore, Md.: 1950), 2007, 178: 4473-4481.
[37] Hsu JL, vandenBoomen DJH, Tomasec P, et al. Plasma membrane profiling defines an expanded class of cell surface proteins selectively targeted for degradation by HCMV US2 in cooperation with UL141. PLoS pathogens, 2015, 11: e1004811.
[38] Orange JS, Fassett MS, Koopman LA, et al. Viral evasion of natural killer cells. Nature Immunology, 2002, 3: 1006-1012.
[39] Almeida GWC, Oliveira MT, Martines IGL, et al. Expression profile of human cytomegalovirus UL111A cmvIL-10 and LAcmvIL-10 transcripts in primary cells and cells from renal transplant recipients. Viruses, 2025, 17: 501.
[40] Mattes FM, McLaughlin JE, Emery VC, et al. Histopathological detection of owl’s eye inclusions is still specific for cytomegalovirus in the era of human herpesviruses 6 and 7. Journal of Clinical Pathology, 2000, 53: 612-614.
[41] Salomè S, Corrado FR, Mazzarelli LL, et al. Congenital cytomegalovirus infection: The state of the art and future perspectives. Frontiers in Pediatrics, 2023, 11: 1276912.
[42] Shang Z, Li X. Human cytomegalovirus: Pathogenesis, prevention, and treatment. Molecular Biomedicine, 2024, 5: 61.
[43] Gault E, Michel Y, Dehée A, et al. Quantification of human cytomegalovirus DNA by real-time PCR. Journal of Clinical Microbiology, 2001, 39: 772-775.
[44] Ho SKN, Lo CY, Cheng IKP, et al. Rapid cytomegalovirus pp65 antigenemia assay by direct erythrocyte lysis and immunofluorescence staining. Journal of Clinical Microbiology, 1998, 36: 638-640.
[45] Bert PJ, Narvaez Gaitan CA, VasquezVado VE. Congenital cytomegalovirus in a resource-limited setting: A case report. Cureus, 16: e62844.
[46] Anyfantakis D, Damianaki A, Krietsepi V, et al. A fatal case of cytomegalovirus disease in an immunocompetent young woman: A case report. Le Infezioni in Medicina, 2018, 26: 164-166.
[47] Hamilton ST, van Zuylen W, Shand A, et al. Prevention of congenital cytomegalovirus complications by maternal and neonatal treatments: A systematic review. Reviews in Medical Virology, 2014, 24: 420-433.
[48] Engelmann C, Sterneck M, Weiss KH, et al. Prevention and management of CMV infections after liver transplantation: Current practice in german transplant centers. Journal of Clinical Medicine, 2020, 9: 2352.
.png)
