1.输血传播病毒(Torque teno virus, TTV)
物种名:输血传播病毒
拉丁学名:Torque teno virus(TTV)
分类学地位:单链DNA病毒界Monodnaviria;Cossaviricota门Cossaviricota;Arfiviricetes纲Arfiviricetes;Arfivirales目Arfivirales; 环病毒科Anelloviridae;α扭转病毒属Alphatorquevirus
输血传播病毒通常称为Torque teno virus,是一种在全球范围内广泛感染人类和多种动物的微小病毒。输血传播病毒于1997年由日本科学家Nishizawa等人在一例非甲-非庚型输血后肝炎患者血清中首次发现,并因此得名。输血传播病毒具有极高的感染性,可通过血液、粪便、呼吸道分泌物等途径传播[1]。输血传播病毒在世界卫生组织(WHO)生物安全分级中为生物安全等级2级(Biosafety Level 2, BSL-2)标准[6]。
1.1生物学特性
1.1.1培养特征
输血传播病毒至今没有稳定、高效、标准化的体外培养系统,缺乏易感的永生化细胞系,并且具有高度的变异性导致其难以培养。
1.1.2形态学特征
输血传播病毒是指环病毒目中最具代表的成员,输血传播病毒是无包膜的二十面体对称的球形颗粒,病毒颗粒直径约30-32 nm[2]。
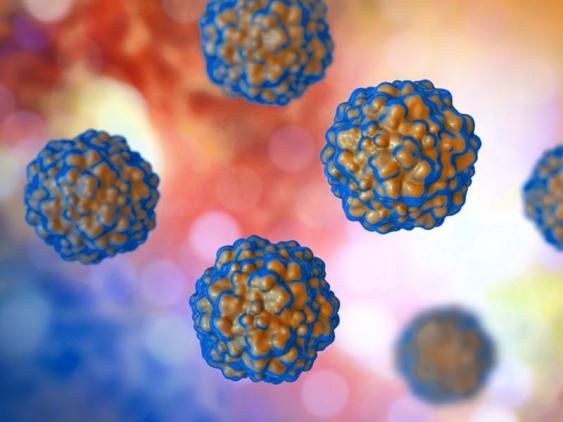
图1 TTV模式图
1.1.3生化特征
输血传播病毒在氯化铯梯度离心中,其浮密度为1.31-1.35 g/cm3,这是无包膜的病毒特征,由于其缺乏脂质包膜,它对有机溶剂(如乙醚、氯仿)具有抵抗力,在环境中相对稳定[2]。
1.1.4分子生物学特征
TTV是一种单股环状负链无包膜DNA病毒(ssDNA),该病毒DNA由3852个核苷酸组成,基因组分编码区和非编码区,编码区占70%,非编码区占30%。其基因组中包含三个ORFs片段,长的ORF1和短的ORF2,ORF3则是在ORF1下游与ORF2重叠的部分[3]。TTV还有很强的变异性,有至少三十几种不同基因型。
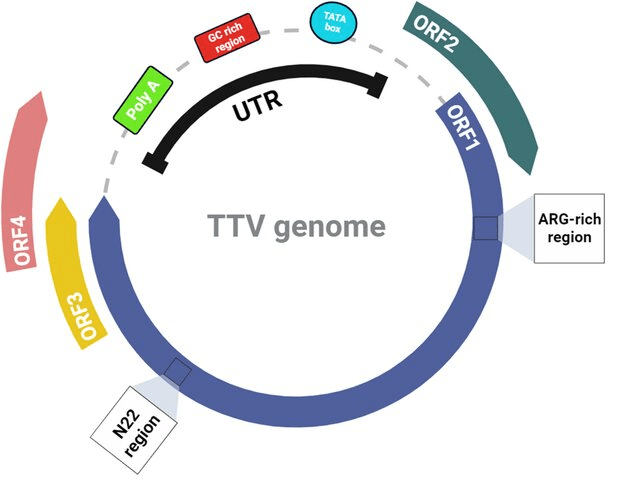
图2 TTV基因组结构
1.2分布、传播与致病性
1.2.1分布与传播
TTV感染遍布全世界,无论是在发达国家还是发展中国家,都有它的踪迹,没有明显的地域性聚集。绝大多数的感染者表现为无症状携带状态,病毒在血液和组织中持续存在,形成慢性感染。TTV并非是人类特有的,在很多家畜和宠物中都发现了不同类型的TTV病毒[4]。输血传播病毒可通过粪-口途径传播、呼吸道传播及血液和体液传播,在感染者的粪便、呼吸道分泌物、血液、人奶、精液和宫颈分泌液中都能检测TTV病毒颗粒[5]。
1.2.2致病性
TTV在全球健康成人中的感染率很高,且无明显疾病症状,研究表明TTV与多种常见疾病包括肝炎、呼吸道疾病、癌症、自身免疫病等都无因果关系[6]。有研究表明在器官移植、HIV/AIDS等免疫抑制患者中,TTV病毒的载量通常极高。这可能表明TTV的载量可能作为免疫监测生物标志物,而非直接的致病因子[7]。
1.3检测方法
最常用的TTV检测方法是巢氏PCR法:通过扩增高度保守的UTR区域,以提高检测灵敏度和广度,能检测出更多基因型。首先采集血浆或血清样本,使用核酸提取出包括TTV DNA在内的总核酸,使用半巢氏PCR和巢氏PCR两轮扩增片段,随后进行凝胶电泳验证并测序确定其基因型[8]。
表1 半巢氏PCR序列[8]
| 名称 | 序列 |
| F | 5′-GCAAGCAGCATCAGGACAGG-3′ |
| R | 5′-CTGGCATTTTACCATTTCCAAAGTT-3′ |
表2 巢氏PCR序列[8]
| 名称 | 序列 |
| F | 5′-CGAAACCTGGTAAGGTACGG-3′ |
| R | 5′-CTGGCATTTTACCATTTCCAAAGTT-3′ |
1.4典型案例
巴西南部3个学校收集的自来水中检测出TTV。研究结果表明,污水处理量的百分比与TTV基因组的检出率呈现轻微负相关(r=-0.76)。TTV检出率与大肠埃希氏菌检出率有较强的相关性(r=0.97),表明TTV可能是粪便污染的合适标志[9]。
1.5防治对策
尽管TTV没有明确的致病性,但是仍然有许多传播途径,对于血浆制品进行灭活处理,注意个人卫生,饭前便后用肥皂和清水洗手。饮用干净水源食用干净食品,避免静脉注射吸毒和不安全的性行为等高危行为。
参考文献
- Nishizawa T, Okamoto H, Konishi K et al. A novel DNA virus (TTV) associated with elevated transaminase levels in posttransfusion hepatitis of unknown etiology. Biochem Biophys Res Commun, 1997, 241: 92-7.
- Okamoto H. History of discoveries and pathogenicity of TT viruses. Curr Top Microbiol Immunol, 2009, 331: 1-20.
- 傅海霞, 王志钢. 输血传播病毒分子生物学研究进展. 生物技术通报, 2011: 68-70.
- Spandole S, Cimponeriu D, Berca LM et al. Human anelloviruses: an update of molecular, epidemiological and clinical aspects. Arch Virol, 2015, 160:893-908.
- Ross RS, Viazov S, Runde V et al. Detection of TT virus DNA in specimens other than blood. J Clin Virol, 1999, 13: 181-4.
- Maggi F, Bendinelli M. Immunobiology of the Torque teno viruses and other anelloviruses. Curr Top Microbiol Immunol, 2009, 331:65-90.
- De Vlaminck I, Khush KK, Strehl C et al. Temporal response of the human virome to immunosuppression and antiviral therapy. Cell, 2013, 155: 1178-87.
- Takahashi K, Iwasa Y, Hijikata M et al. Identification of a new human DNA virus (TTV-like mini virus, TLMV) intermediately related to TT virus and chicken anemia virus. Arch Virol, 2000, 145: 979-93.
- Vecchia AD, Kluge M, dos Santos da Silva JV et al. Presence of Torque teno virus (TTV) in tap water in public schools from Southern Brazil. Food Environ Virol, 2013, 5: 41-5.
.png)
